题目内容
2.实验室有两瓶标签被腐蚀的无色溶液,老师告知分别是“氯化钠和盐酸”,请你分别用三种不同原理的方法将其鉴别?分析 首先分析两种物质的组成和类别,氯化钠是盐,盐酸是酸;鉴别盐酸可根据其酸性等性质进行试剂的选择;题意要求三种方法的现象不一,常见的现象主要颜色、生成沉淀或放出气体.
解答 解:①因为盐酸呈酸性,所有可用紫色石蕊试液检验,变红色,而氯化钠不变色;
②因为盐酸是酸可和活泼的金属反应放出氢气,可用锌粒进行检验,和盐酸反应有气泡产生;
③因为碳酸钠能够和盐酸反应产生气泡,氯化钠没有.
同理还可选用氧化铜、氢氧化铜等试剂都可鉴别出.
故答案为:①石蕊试液; ②锌粒;③碳酸钠(或氧化铜、氢氧化铜等).
点评 本题主要考查学生根据物质性质进行鉴别的内容,对于本题还要注意审题,题干要求所举三个试剂反应后的现象不同,这是本题的难点.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
13.对下列知识的归纳,都正确的一组是( )
| A. | 生活常识 取暖防中毒--煤炉上放一盆水 炒菜时油锅着火--用锅盖盖灭 | |
| B. | 节约意识 用剩药品--应放回原瓶 取用药品--应取少量 | |
| C. | 安全常识 厨房煤气泄漏--打开排气扇 家用电器着火--用水浇灭 | |
| D. | 环保意识 使用含磷洗衣粉--含污染水源 减少白色污染--使用可降解塑料 |
10.下列物质中,前者属于氧化物,后者属于混合物的是( )
| A. | 氧气和空气 | B. | 水和空气 | C. | 过氧化氢和液氧 | D. | 空气和臭氧 |
7.下列图示的实验中涉及到化学变化的是( )
| A. | 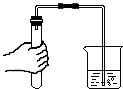 检查装置的气密性 | B. | 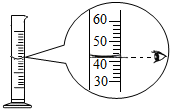 读取水的体积 | ||
| C. | 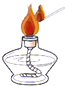 点燃酒精灯 | D. |  活性炭吸附红棕色二氧化氮 |
14.小明是热爱生活、爱好化学的学生,下列是他平时的部分观察、记录、分析、总结,其中不科学的是( )
| A. | 金刚石、石墨物理性质差异很大是因为它们的结构中碳原子的排列方式不同 | |
| B. | 古代的名家字画,留传至今,是因为碳单质常温下化学性质稳定 | |
| C. | 干冰用于人工降雨是因为干冰易升华同时吸收大量的热量 | |
| D. | 发现家里煤气泄漏时,应立即打开排气扇 |