题目内容
20.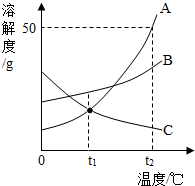 A、B、C三种物质的溶解度曲线如图所示.请回答:
A、B、C三种物质的溶解度曲线如图所示.请回答:(1)t1℃时,A、B、C三种物质的溶解度由大到小是B>A=C.
(2)t2℃时,把30gA放入50g水中,充分搅拌能得到A 溶液的质量是75g.
(3)将C物质的不饱和溶液变为饱和溶液,可采用加入C物质(合理均可) 的方法(任写一种).
(4)将t2℃时,A、B、C三种物质的饱和溶液均降温至t1℃,所得溶液的溶质质量分数的大小关系是B>A>C.
分析 (1)根据固体的溶解度曲线可以:比较不同物质在同一温度下的溶解度大小;
(2)可查出某物质在一定温度下的溶解度,从而确定溶液的质量;
(3)可知物质的溶解度随温度变化的变化情况,从而判断不饱和溶液转化为饱和溶液的方法;
(4)据饱和溶液中溶质的质量分数计算方法及物质的溶解度随温度变化情况分析解答.
解答 解:(1)t1℃时,A、B、C三种物质的溶解度由大到小是 B>A=C;
(2)t2℃时A的溶解度是50g,即100g水中最多溶解50g的A,则把30gA放入50g水中,充分搅拌最多溶解25g,能得到A 溶液的质量是75g;
(3)C的溶解度随温度升高而减小,所以将C物质的不饱和溶液变为饱和溶液,可采用 加入溶质或蒸发溶剂、升温的方法;
(4)将t2℃时,A、B、C三种物质的饱和溶液均降温至t1℃,AB析出晶体,则溶质的质量分数减小,C的溶解度变大,溶液的组成不变,溶质的质量分数与降温前相等;饱和溶液中溶质的质量分数的计算式是:$\frac{溶解度}{溶解度+100g}$×100%,则溶解度大溶质的质量分数大,而t1℃B的溶解度大于A的溶解度大于降温前C的溶解度,故所得溶液的溶质质量分数的大小关系是(2)t1℃时,b物质的溶解度最大,a物质次之,a、b物质的溶解度随温度的降低而减小,会析出晶体,c物质的降低温度不会析出晶体,c物质应该按照t2℃时的溶解度计算,所以将t2℃时,a、b、c三种物质的饱和溶液降温至t1℃时,所得溶液溶质质量分数由大到小的顺序是B>A>C;
故答案为:(1)B>A=C;(2)75;(3)加入C物质(合理均可);(4)B>A>C.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

| A. | +4 | B. | +6 | C. | +2 | D. | +3 |
| A. | 现象:将一粒金属钾加入氯化铜溶液会产生气体、蓝色沉淀和少量不溶性黑色固体 | |
| B. | 设计:验证久置空气的NaOH是否变质,可将固体溶于水并加入酚酞试液观察颜色 | |
| C. | 操作:石蕊试纸和pH试纸使用前都必须用蒸馏水润湿 | |
| D. | 步骤:探究H2还原氧化铜反应时,实验结束时应先停止通H2,再移去酒精灯 |
| A | 食品安全 | B | 化学知识的应用 |
| 自来水加漂白粉--杀菌消毒 食用加碘盐--预防贫血 干冰冷藏食品--升华吸热 | 住宅着火时用水扑灭-降低着火点 点燃可燃性气体前要验纯--避免爆炸 自行车架防锈--涂漆 | ||
| C | 日常物质的区别 | D | 化学之“最” |
| 硬水和软水-加肥皂水搅拌 食盐水和糖水--尝味道 合成纤维和羊毛--点燃闻气味 | 空气中含量最多的气体-O2 最硬的矿物质--金刚石 地壳中含量最多的金属元素Al |
| A. | A | B. | B | C. | C | D. | D |
| 物质 | 实验目的 | 实验操作 | |
| A | CO2中含有少量CO | 除杂 | 通过灼热的氧化铜 |
| B | MnO2和KCl的混合物 | 分离 | 溶解、过滤、蒸发;滤渣洗涤、干燥 |
| C | 氧气和氮气 | 鉴别 | 带火星的木条 |
| D | Na2CO3溶液中可能含有NaOH | 检验 | 酚酞试液 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 石碱 | B. | 烧碱 | C. | 熟石灰 | D. | 氨水 |
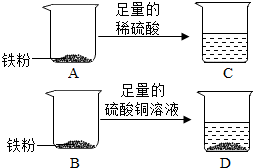 实验室有一包纯净的铁粉,小明为了探究金属的化学性质并测定铁的相对原子质量,设计了如图所示的实验.
实验室有一包纯净的铁粉,小明为了探究金属的化学性质并测定铁的相对原子质量,设计了如图所示的实验. 小明用图甲所示装置测定空气中氧气的含量.
小明用图甲所示装置测定空气中氧气的含量.