题目内容
13.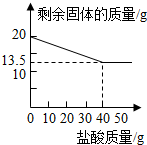 某化学兴趣小组的同学为测定假黄金(铜锌合金)组成元素的质量分数,称取20克假黄金置于烧杯中,用某浓度的稀盐酸50克,分5次加入,每次充分反应后,取出固体,经过滤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量的关系如图所示:
某化学兴趣小组的同学为测定假黄金(铜锌合金)组成元素的质量分数,称取20克假黄金置于烧杯中,用某浓度的稀盐酸50克,分5次加入,每次充分反应后,取出固体,经过滤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量的关系如图所示:(1)求铜锌合金中锌的质量分数;
(2)从图可知,当所用合金与稀盐酸的质量比为1:2时,表明锌恰好完全溶解;
(3)计算稀盐酸中溶质的质量分数.
分析 (1)剩余固体是铜,根据铜的质量和假黄金的质量可以计算出合金中锌的质量分数;
(2)由曲线图可知,加入40g盐酸后恰好完全反应,剩余13.5g铜,根据铜的质量和假黄金的质量来计算合金与盐酸的质量比;
(3)由锌和完全反应时盐酸的质量根据锌与盐酸反应的化学方程式可以计算出稀盐酸中溶质的质量分数和生成氯化锌、氢气的质量.
解答 解:(1)锌和盐酸反应,而铜和盐酸不反应,加入过量盐酸后,剩余固体为铜,
铜的质量为13.5g;锌的质量=20g-13.5g=6.5g
合金中锌的质量分数为$\frac{6.5g}{20g}$×100%=32.5%
(2)由曲线图可知,加入40g盐酸后恰好完全反应,剩余13.5g铜,此时合金与稀盐酸的质量比=20:40=1:2,所以当所用合金与稀盐酸的质量比为1:2时,表明锌恰好完全溶解;
(3)设6.5g锌与质量为x的氯化氢恰好完全反应
Zn+2HCl=ZnCl2+H2↑
65 73
6.5g x
$\frac{65}{6.5g}$=$\frac{73}{x}$,x=7.3g
稀盐酸的质量分数=$\frac{7.3g}{40g}$×100%=18.25%
答:(1)合金中锌的质量分数为32.5%.
(2)从图可知,当所用合金与稀盐酸的质量比为1:2时,表明锌恰好完全溶解.
(3)稀盐酸中溶质的质量分数为18.25%.
点评 本题主要考查学生利用化学方程式和溶质质量分数公式进行计算的能力,解题时要知道铜与稀盐酸不反应,铜锌合金与稀盐酸的反应,为锌与稀盐酸的反应,然后根据化学方程式进行计算,问题即可迎刃而解.

练习册系列答案
相关题目
4.甲醛是一种有毒物质,可用作农药和消毒剂,下列关于甲醛(CH2O)的说法错误的是( )
| A. | 从类别上看:甲醛属于有机物 | |
| B. | 从变化上看:甲醛完全燃烧生成水和二氧化碳 | |
| C. | 从宏观上看:甲醛由碳、氢、氧三种元素组成 | |
| D. | 从微观上看:甲醛由1个碳原子、2个氢原子和1个氧原子构成 |
8.对于下列几种化学符号,有关说法正确的是( )
①H ②Fe2+ ③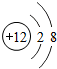 ④P205 ⑤KClO3.
④P205 ⑤KClO3.
①H ②Fe2+ ③
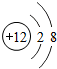 ④P205 ⑤KClO3.
④P205 ⑤KClO3.| A. | 表示物质组成的化学式有①④⑤ | |
| B. | ④中数字“5”表示五氧化二磷中有5个氧原子 | |
| C. | 表示阳离子的有②③ | |
| D. | ⑤中氯元素的化合价为-1 |
5.下列事实的结论或解释中不正确的是( )
| A. | 水烧开后易把壶盖充起--说明温度升高分子变大 | |
| B. | 公园的桂花开放时满园飘香--说明分子在不断运动 | |
| C. | 水通电分解成氢气和氧气--实质是分子分解成原子,原子重新组合成新的分子 | |
| D. | 过生日时,小明吹灭生日蜡烛--灭火的原理时使温度降到着火点以下 |
2.下列各组溶液中不用其他试剂,仅用组内物质及相互反应就能区别开来的是( )
| A. | Na2CO3 H2SO4 HCl K2SO4 | B. | K2CO3 BaCl2 HNO3 H2SO4 | ||
| C. | HCl AgNO3 HNO3 NaCl | D. | NaOH CuSO4 K2SO4 NaCl |
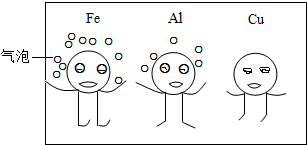 为验证Cu、Al、Fe三种金属的活动性顺序,有甲、乙、丙三位同学设计了如下方案:(溶液中Fe2+浅绿色、Cu2+蓝色、Al3+无色)
为验证Cu、Al、Fe三种金属的活动性顺序,有甲、乙、丙三位同学设计了如下方案:(溶液中Fe2+浅绿色、Cu2+蓝色、Al3+无色)