题目内容
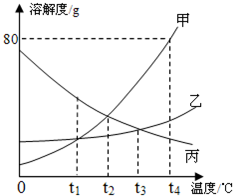 根据甲、乙、丙三种固体物质的溶解度曲线回答:
根据甲、乙、丙三种固体物质的溶解度曲线回答:(1)随温度的升高其溶解度反而减小的是
(2)在t4℃时,甲物质的100g饱和溶液中,溶质、溶剂、溶液的质量比是
(3)t4℃时,质量相等的甲、乙、丙三杯饱和溶液中,溶质质量分数的大小关系是
考点:固体溶解度曲线及其作用,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)根据溶解度曲线图AB物质的溶解度随温度的升高而增大,C物质的溶解度随温度的升高而减小;根据溶解度曲线可知,t1℃时A和B的曲线相交,两者的溶解度相等;
(2)根据t4℃时,甲物质的溶解度解答;
(3)根据甲、乙、丙三种物质的溶解度曲线,某温度下物质的饱和溶液的溶质质量分数的比较.
(2)根据t4℃时,甲物质的溶解度解答;
(3)根据甲、乙、丙三种物质的溶解度曲线,某温度下物质的饱和溶液的溶质质量分数的比较.
解答:解:
(1)根据溶解度曲线图AB物质的溶解度随温度的升高而增大,C物质的溶解度随温度的升高而减小,故填C;
根据溶解度曲线可知,t1℃时A和B的曲线相交,两者的溶解度相等,都小于C 的溶解度;
(2)t4℃时,甲物质的溶解度为80g.即此温度时,100g水溶解甲物80g形成此温度下的180g饱和溶液;所以此温度下100g甲物质的饱和溶液中,溶质的质量为
=
g,溶剂的质量为100g-
g=
g,溶质、溶剂、溶液的质量比为
g:
g:100g.故答:4:5:9;
(3)t4℃时,甲、乙、丙物质的溶解度是甲>乙>丙,即此温度时,质量相等饱和溶液中溶解甲、乙、丙物质的质量甲>乙>丙,所以t4℃时三种物质的饱和溶液中,溶质质量分数的大小关系为甲>乙>丙;溶解度越大,所需的溶剂越少,所以把这三杯饱和溶液的温度都降到t2℃,此时烧杯中溶剂最多的是丙.
答案:
(1)丙;t1;
(2)4:5:9;
(3)甲>乙>丙; 丙.
(1)根据溶解度曲线图AB物质的溶解度随温度的升高而增大,C物质的溶解度随温度的升高而减小,故填C;
根据溶解度曲线可知,t1℃时A和B的曲线相交,两者的溶解度相等,都小于C 的溶解度;
(2)t4℃时,甲物质的溶解度为80g.即此温度时,100g水溶解甲物80g形成此温度下的180g饱和溶液;所以此温度下100g甲物质的饱和溶液中,溶质的质量为
| 80g×100g |
| 180g |
| 400 |
| 9 |
| 400 |
| 9 |
| 500 |
| 9 |
| 400 |
| 9 |
| 500 |
| 9 |
(3)t4℃时,甲、乙、丙物质的溶解度是甲>乙>丙,即此温度时,质量相等饱和溶液中溶解甲、乙、丙物质的质量甲>乙>丙,所以t4℃时三种物质的饱和溶液中,溶质质量分数的大小关系为甲>乙>丙;溶解度越大,所需的溶剂越少,所以把这三杯饱和溶液的温度都降到t2℃,此时烧杯中溶剂最多的是丙.
答案:
(1)丙;t1;
(2)4:5:9;
(3)甲>乙>丙; 丙.
点评:溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同;了解结晶的原理、方法及其应用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列实验操作正确的是( )
A、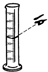 读液体体积 |
B、 引燃酒精灯 |
C、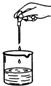 滴加液体 |
D、 取固体药品 |
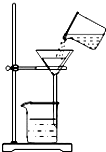 我县某化学兴趣小组的同学用洁净的塑料瓶从清河中取回一定量的水样,然后进行如下研究分析:
我县某化学兴趣小组的同学用洁净的塑料瓶从清河中取回一定量的水样,然后进行如下研究分析: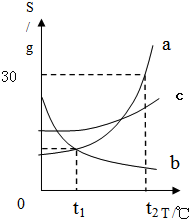 如图是a、b、c三种物质的溶解度曲线
如图是a、b、c三种物质的溶解度曲线