题目内容
5.将金属钠放入水中,得到 NaOH溶液并放出H2.(1)计算将10g Na放入90g水中所得溶液溶质的质量分数.(精确到0.1%)
(2)若将10g ①Na、②NaOH、③Na2O分别放入90g水中,所得溶液的浓度由大到小的顺序是①③②(请用序号表示).
分析 根据钠与水反应生成氢氧化钠和氢气的方程式算出反应后溶质氢氧化钠的质量,再算出氢气质量,再计算出溶液质量,根据计算公式再算出所得溶液的质量分数.
解答 解:(1)设10克金属钠与水反应生成氢氧化钠的质量为X,生成氢气质量为Y,
2Na+2H2O═2NaOH+H2↑
46 80 2
10g X Y
根据:$\frac{46}{10g}$=$\frac{80}{X}$
$\frac{46}{10g}$=$\frac{2}{Y}$
解得X=17.4g;Y=0.4g,
反应后所得溶液的质量分数:$\frac{17.4g}{10g+90g-0.4g}$×100%=17.5%;
(2)根据溶质与溶液的质量关系分析:钠溶于水时,10gNa转化为17.4gNaOH,对应溶液的质量为99.6g<100g;
NaOH溶于水时,10gNaOH对应溶液的质量为100g;
Na2O溶于水时,10gNa2O转化为12.9gNaOH,对应溶液的质量为100g;
所以所得溶液的浓度由大到小的顺序是①③②.
点评 通过回答本题知道了有的物质放入水中溶质已经变了,要根据方程式算出溶质质量再进行计算.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目


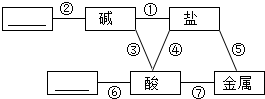 归纳是学习的重要方法,在学习酸、碱、盐后,绘制出如图所示的物质之间的反应关系,(图中短线连接的物质表示能相互反应),请填写下列空白:
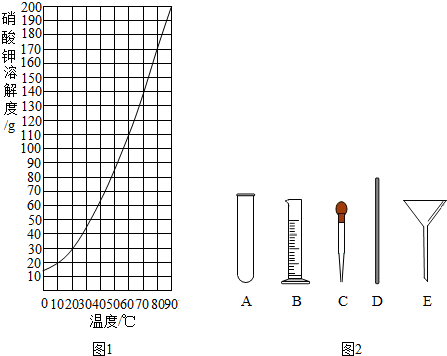
归纳是学习的重要方法,在学习酸、碱、盐后,绘制出如图所示的物质之间的反应关系,(图中短线连接的物质表示能相互反应),请填写下列空白: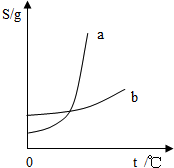 硝酸钾是初中化学常见的一种盐.请按要求填写下列有关空格:
硝酸钾是初中化学常见的一种盐.请按要求填写下列有关空格: