题目内容
5.根据质量守恒定律可知,对反应2A2+B2=2M来说,M的化学式应是A2B.分析 由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物M的化学式.
解答 解:由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式2A2+B2=2M,反应前A、B原子个数分别为4、2,反应后的生成物中A、B原子个数分别为0、0,根据反应前后原子种类、数目不变,则2M分子中含有4个A原子和2个B原子,则每个M分子由2个A原子和1个B原子构成,则物质M的化学式为A2B.
故答案为:A2B.
点评 本题难度不大,掌握利用化学反应前后原子守恒来确定物质的化学式的方法是正确解答此类题的关键.

练习册系列答案
 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
9. 如图是三种微粒的结构示意图,有关它们的说法正确的是( )
如图是三种微粒的结构示意图,有关它们的说法正确的是( )
 如图是三种微粒的结构示意图,有关它们的说法正确的是( )
如图是三种微粒的结构示意图,有关它们的说法正确的是( )| A. | 它们属于同种元素的微粒 | B. | 它们都是原子 | ||
| C. | 它们原子的最外层电子数相同 | D. | 它们原子的电子层不完全相同 |
10.下列物质在空气中易潮解的是( )
| A. | 浓硫酸 | B. | NaOH溶液 | C. | 粗食盐 | D. | 硝酸钠 |
17.使用托盘天平.若指针偏右就进行称量,则称量结果与实际质量相比( )
| A. | 偏大 | B. | 偏小 | C. | 相等 | D. | 无法确定 |
14.石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下表:
(1)该石灰石样品中碳酸钙的质量分数是75%;
(2)煅烧这种石灰石样品100t,最多能制得生石灰多少?
(3)计算该稀盐酸的溶质质量分数(指这20g的稀盐酸中HCl所占的百分含量)
(后二小题应写出计算过程,结果精确到0.1%).
| 稀盐酸的用量 | 第一次加入5g | 第二次加入5g | 第三次加入5g | 第四次加入5g |
| 剩余固体的质量 | 3g | 2g | l g | 1g |
(2)煅烧这种石灰石样品100t,最多能制得生石灰多少?
(3)计算该稀盐酸的溶质质量分数(指这20g的稀盐酸中HCl所占的百分含量)
(后二小题应写出计算过程,结果精确到0.1%).
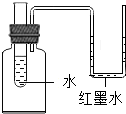 如图所示的装置中,加入氢氧化钠固体,片刻后U型管中左侧液面将下降(填上升、下降或不变),产生这一现象的原因是向水中加入的氢氧化钠溶于水时放热,使瓶内气体压强增大.若用代替氢氧化钠固体,U型管中液面会出现相反的现象.
如图所示的装置中,加入氢氧化钠固体,片刻后U型管中左侧液面将下降(填上升、下降或不变),产生这一现象的原因是向水中加入的氢氧化钠溶于水时放热,使瓶内气体压强增大.若用代替氢氧化钠固体,U型管中液面会出现相反的现象. 人体通过肺与外界进行气体交换,吸入空气 中的氧气,排出二氧化碳和水蒸气.但人体排出的二氧化碳究竟是空气中原有的,还是人体代谢的最终产物?为了证实这个问题,有人采用了如图所示装置进行实验.
人体通过肺与外界进行气体交换,吸入空气 中的氧气,排出二氧化碳和水蒸气.但人体排出的二氧化碳究竟是空气中原有的,还是人体代谢的最终产物?为了证实这个问题,有人采用了如图所示装置进行实验.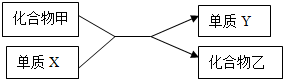 根据如图化合物与单质相互转化的关系回答:
根据如图化合物与单质相互转化的关系回答: