题目内容
5.实验室用过氧化氢制取氧气的变化可用下式表示:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气
(1)上述变化所涉及的物质中,属于金属氧化物的是Mn02(写化学式,下同),其中氧元素的化合价为-1价的物质是H2O2(填化学式);该物质是纯净物(填纯净物或混合物).
(2)实验中,加入少量二氧化锰的作用是加快反应速率(或催化作用);若未加入二氧化锰,则反应明显减慢(选填“不能发生”或“明显减慢”).
分析 (1)根据氧化物的定义及金属氧化物的特点分析;根据化合物中化合价的代数和为0回答;
(2)根据催化剂的作用分析回答:改变化学反应的速率,而本身的质量和化学性质在反应前后都没有发生改变.
解答 解:(1)在过氧化氢的分解的变化过程中,涉及到的物质有:过氧化氢、二氧化锰、水和氧气,其中过氧化氢、二氧化锰和水都是由两种元素组成,且含有氧元素的化合物,即氧化物,但属于金属氧化物的是二氧化锰;这四种物质中都含有氧元素,其中氧气中氧元素的化合价为0,二氧化锰和水中氧元素的化合价都是-2,只有过氧化氢中氧元素的化合价是-1,过氧化氢属于纯净物;
(2)用氯酸钾或过氧化氢制取氧气的实验中,都需要加入少量二氧化锰,二氧化锰在这儿作为催化剂,因此二氧化锰的作用是加快反应速率(或催化作用); 若未加入二氧化锰,则反应明显减慢,不会影响氧气的产量.
故答案为:(1)Mn02;H2O2;纯净物;
(2)加快反应速率(或催化作用);明显减慢.
点评 本题是有关氧气的两种不同的制取方法的探究,考查了物质的分类、元素的化合价、催化剂的作用、及有关方程式的计算,难度不大,依据已有的知识即可完成.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
13.如图所示的化学实验基本操作错误的是( )
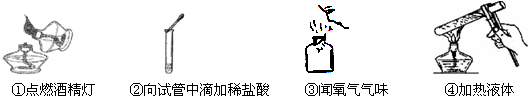

| A. | ①②③ | B. | ①②④ | C. | ②③④ | D. | ①②③④ |
10.某化合物由A,B两种元素组成,已知A、B两元素的质量比为7:4,相对原子质量之比为7:8,则此化合物分子式可能是( )
| A. | A2B | B. | AB | C. | AB2 | D. | A2B4 |
17.葡萄糖(化学式:C6H12O6)在生物学领域具有重要地位,是活细胞的能量来源和新陈代谢中间产物,即生物的主要供能物质.下列关于葡萄糖的说法正确的是( )
| A. | 葡萄糖是氧化物 | |
| B. | 葡萄糖中C、H、O三种元素的质量比为6:12:6 | |
| C. | 葡萄糖由6个碳元素、12个氢元素、6个氧元素构成 | |
| D. | 葡萄糖的相对分子质量为:180 |
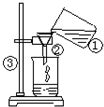 指出如图装置中几处错误:错误①缺少玻璃棒引流②漏斗下端没有紧靠在烧杯内壁上③滤液高于滤纸边缘,经过滤后滤液仍然不干净,请分析原因:①滤纸破损②滤液高于滤纸边缘③接滤液的烧杯不干净.
指出如图装置中几处错误:错误①缺少玻璃棒引流②漏斗下端没有紧靠在烧杯内壁上③滤液高于滤纸边缘,经过滤后滤液仍然不干净,请分析原因:①滤纸破损②滤液高于滤纸边缘③接滤液的烧杯不干净.