题目内容
16.某校初三年级在实验室做二氧化碳制取的实验,实验后的废液倒在废液缸中,化学课外活动小组欲对废液的酸碱性及溶质成分进行探究,请你参与设计.(1)反应后溶液中溶质的成分可能是CaCl2,也可能是CaCl2、HCl(写化学式)小马说选用酚酞试液就可检验废液中溶质的成分,你认为是否正确,为什么?不正确,酚酞遇到酸性和中性溶液都不变色.
(2)设计实验进行验证溶液是否呈酸性.(请用两种能写方程式的不同类的方法)
| 实验步骤 | 相关的化学反应方程式 | 结论 |
| 取少量废液加入铁钉 | Fe+2HCl=FeCl2+H2↑ | 溶液呈酸性 |
| 取少量废液加入碳酸钠 | Na2CO3+2HCl=2MaCl+H2O+CO2↑ |
分析 (1)根据盐酸和碳酸钙反应后生成氯化钙,盐酸可能过量,也可能恰好完全反应,酸性和中性溶液都不能使酚酞变色进行分析;
(2)根据盐酸会与活泼金属、碳酸盐等物质反应进行分析;
(3)根据酸的化学性质一般采用中和的方式进行酸液处理进行分析.
解答 解:(1)盐酸和碳酸钙反应后生成氯化钙,盐酸可能过量,也可能恰好完全反应,酸性和中性溶液都不能使酚酞变色,所以反应后溶液中溶质的成分可能是CaCl2,也可能是CaCl2、HCl,选用酚酞试液就可检验废液中溶质的成分的方法不正确,酚酞遇到酸性和中性溶液都不变色;
(2)盐酸会与铁反应生成氯化亚铁和氢气,盐酸会与碳酸钠反应生成氯化钠、水和二氧化碳,所以
| 实验步骤 | 相关的化学反应方程式 | 结论 |
| 取少量废液加入铁钉 | Fe+2HCl=FeCl2+H2↑ | 溶液呈酸性 |
| 取少量废液加入碳酸钠 | Na2CO3+2HCl=2MaCl+H2O+CO2↑ |
故答案为:(1)CaCl2、HCl,不正确,酚酞遇到酸性和中性溶液都不变色;
(2)
| 实验步骤 | 相关的化学反应方程式 | 结论 |
| 取少量废液加入铁钉 | Fe+2HCl=FeCl2+H2↑ | |
| 取少量废液加入碳酸钠 | Na2CO3+2HCl=2MaCl+H2O+CO2↑ |
点评 本题以探究的形式考查溶液的酸碱性的检验,以及实验室废液的处理方法,不但使学生掌握了酸的化学性质还培养了学生的环保意识.

练习册系列答案
相关题目
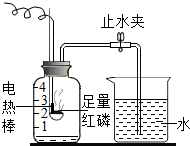 如图是某实验小组测定空气中氧气含量的实验改进装置.
如图是某实验小组测定空气中氧气含量的实验改进装置.
