题目内容
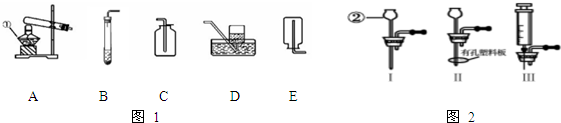
3.如图1是“空气中氧气体积分数测定”实验的改进装置.主要操作是:在实际容积为l50mL的集气瓶里,先装进50mL的水,再按图连好仪器,按下热的玻璃棒,白磷立即被点燃,反应的化学方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.(1)①白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是先下降后升高; 若瓶内水面没有变化,其原因
可能是装置漏气;若实验非常成功,最终集气瓶中水的体积约为70 ml.
②集气瓶里预先装进的50mL水,在实验过程中起到哪些作用是abc(填写序号).
a.加快集气瓶冷却 b.液封导气管末端以防气体逸出 c.缓冲集气瓶内气压的骤然升高
(2)用木炭替代红磷,能否完成上述实验?请简述其原因:不能;木炭在集气瓶中燃烧,生成了二氧化碳气体,集气瓶内气压几乎不变,使集气瓶内外不能形成压强差.
(3)如用图两套装置来测定空气中氧气的体积含量实验时,请结合图示回答有关问题.(已知铜和氧气在加热的条件下反应生成氧化铜)

①根据下表提供的实验数据,完成下表
| 硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
| 25mL | 15mL | 9mL | 15% |
分析 白磷在空气中燃烧是五氧化二磷;
氧气约占空气总体积的五分之一;
实验装置不同,优缺点不同.
解答 解:白磷在空气中燃烧的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
故填:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(1)①白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是先下降后升高;
若瓶内水面没有变化,其原因可能是装置漏气;
集气瓶中氧气的体积约为:100mL×$\frac{1}{5}$=20mL,若实验非常成功,最终集气瓶中水的体积约为:20mL+50mL=70ml.
故填:先下降后升高;装置漏气;70.
②集气瓶里预先装进的50mL水,在实验过程中起到哪些作用是加快集气瓶冷却,液封导气管末端以防气体逸出,缓冲集气瓶内气压的骤然升高
故填:abc.
(2)木炭在集气瓶中燃烧,生成了二氧化碳气体,集气瓶内气压几乎不变,使集气瓶内外不能形成压强差,因此不能用木炭替代红磷.
故填:不能;木炭在集气瓶中燃烧,生成了二氧化碳气体,集气瓶内气压几乎不变,使集气瓶内外不能形成压强差.
(3)①实验测得空气中氧气的体积分数为:$\frac{15mL-9mL}{25mL+15mL}$×100%=15%.
故填:15%.
②装置二更合理,理由是能让空气更易流通,全部通过铜粉,使氧气与铜粉充分反应.
故填:装置二;能让空气更易流通,全部通过铜粉,使氧气与铜粉充分反应.
点评 可以用来测定空气中氧气含量的物质应该具备的条件是:能和空气中的氧气反应,生成物是固体,不能和空气中的其它物质发生化学反应.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
18.下列物质的化学式书写和名称都正确的是( )
| A. | 一氧化碳Co | B. | 氧化硅SiO2 | C. | 氯化钠-NaCl2 | D. | 氧化钠-Na2O |
8.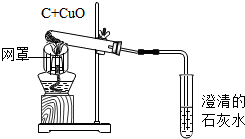 按如图装置进行实验,有关说法及分析不正确的是( )
按如图装置进行实验,有关说法及分析不正确的是( )
 按如图装置进行实验,有关说法及分析不正确的是( )
按如图装置进行实验,有关说法及分析不正确的是( )| A. | 烘干的木炭粉末与CuO粉末须混合均匀 | |
| B. | 网罩的作用是集中火焰,提高温度 | |
| C. | 可观察到澄清石灰水变浑浊 | |
| D. | 结束时先熄灭酒精灯,过一会儿后从液体中取出导管 |
12.圆圆参观某养鱼池时,好奇的发现农民向养鱼池中撒一种叫做过氧化钙的淡黄色固体,用来增加鱼池中的含氧量.小林刚学完氧气的实验室制法,于是他想可否用过氧化钙制取氧气.
[提出问题]过氧化钙可否用于制取氧气?
[查阅资料]部分内容如下:过氧化钙(CaO2)室温下稳定,在300℃时分解生成氧气,可做增氧剂、杀菌剂等.
[猜想与验证]
(1)猜想I:加热过氧化钙可制取氧气.小林依据质量守恒定律,提出猜想I.
[实验与结论]
实验结论:加热过氧化钙可制取氧气.
(2)小林联想到农民用过氧化钙增加鱼池中的含氧量,提出猜想Ⅱ.
猜想Ⅱ:过氧化钙与水反应可制取氧气.
实验结论:反应也能生成氧气,但反应速度慢.
[分析与反思]
①过氧化钙与水反应虽然没有快速收集到大量氧气,但由此实验现象,小明认为农民用过氧化钙做增氧剂的主要原因是过氧化钙在水中持续、缓慢放出氧气,所以可以作为增氧剂.
②小明希望对此实验进行改进,使该反应加快,请你帮他提出合理化建议:加热过氧化钙和水的混合物.
[提出问题]过氧化钙可否用于制取氧气?
[查阅资料]部分内容如下:过氧化钙(CaO2)室温下稳定,在300℃时分解生成氧气,可做增氧剂、杀菌剂等.
[猜想与验证]
(1)猜想I:加热过氧化钙可制取氧气.小林依据质量守恒定律,提出猜想I.
[实验与结论]
| 实验装置 | 实验主要过程 |
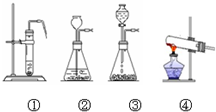 | ①选择实验装置①②③④中的装置④ ②检验装置气密性. ③加入过氧化钙,加热,导管口有大量气泡冒出. ④收集满一瓶气体. ⑤检验气体. |
(2)小林联想到农民用过氧化钙增加鱼池中的含氧量,提出猜想Ⅱ.
猜想Ⅱ:过氧化钙与水反应可制取氧气.
| 实验装置 | 实验主要过程 |
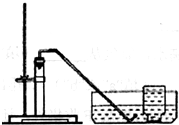 | ①检验装置气密性. ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体.该装置放置到第二天,集气瓶中只收集到极少量气体,震荡试管后仍有少量细小气泡缓慢放出. |
[分析与反思]
①过氧化钙与水反应虽然没有快速收集到大量氧气,但由此实验现象,小明认为农民用过氧化钙做增氧剂的主要原因是过氧化钙在水中持续、缓慢放出氧气,所以可以作为增氧剂.
②小明希望对此实验进行改进,使该反应加快,请你帮他提出合理化建议:加热过氧化钙和水的混合物.