题目内容
7.实验是进行科学探究的重要方法,化学兴趣小组的同学设计如下实验: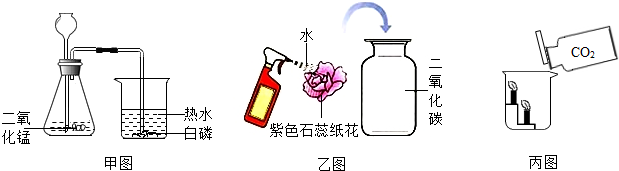
(1)甲图中,欲使热水中的白磷燃烧起来,长颈漏斗应加入的药品是H2O2;
(2)乙图的纸花喷水后放入二氧化碳中,可观察到的现象是紫色纸花变红色,这是因为二氧化碳与水反应生成碳酸的缘故.丙图实验观察到的现象可以说明该气体具有的性质是密度比空气大且不支持燃烧,此性质决定该气体的用途是用来灭火.
分析 (1)根据燃烧的条件分析;
(2)二氧化碳与水化合生成碳酸,碳酸显酸性,据此分析回答;根据实验的现象分析性质.
解答 解:(1)欲使热水中的白磷燃烧起来,就要通入氧气,所以长颈漏斗应加入的药品是双氧水,双氧水在二氧化锰催化作用下生成氧气;
故答案为:H2O2;
(2)由于二氧化碳能与水化合生成了碳酸,碳酸显酸性.所以乙图中将纸花喷水后放入二氧化碳中观察到纸花变红色,发生该现象的化学原理是:水+二氧化碳→碳酸.
丙图装置中通入的气体为二氧化碳,可以看到的现象是:下面的蜡烛先熄灭,上面的蜡烛后熄灭,说明二氧化碳所具有的性质是:密度比空气大、不燃烧不支持燃烧,所以二氧化碳可用于灭火.
故答案为:紫色纸花变红色;碳酸;密度比空气大且不支持燃烧;灭火.
点评 本题的难度不大,主要考查了燃烧的条件、二氧化碳的性质,属于基础的知识,难度不大.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案
相关题目
17.对知识进行归纳总结是一种重要的学习方法,以下说法正确的是( )
①有机物都是含碳化合物;②带电微粒都是离子;③生成盐和水的反应都是中和反应;④混合物都有多种元素组成;⑤溶液都均一、稳定;⑥合金至少含一种金属;⑦能使酚酞变红的溶液,一定是碱的溶液.
①有机物都是含碳化合物;②带电微粒都是离子;③生成盐和水的反应都是中和反应;④混合物都有多种元素组成;⑤溶液都均一、稳定;⑥合金至少含一种金属;⑦能使酚酞变红的溶液,一定是碱的溶液.
| A. | ①②④⑤ | B. | ①⑤⑥ | C. | ①②⑥ | D. | ②④⑥⑦ |
18.有关资源、能源、环境的叙述正确的是( )
| A. | 空气是一种宝贵的能源,空气污染是来自于化石燃料的燃烧 | |
| B. | 地球上的水储量是丰富的,所以淡水资源也极其丰富 | |
| C. | 回收废旧金属不仅能节约金属资源,还能节约能源和保护环境 | |
| D. | 可燃冰主要成分是甲烷,属于化石燃料,目前开发成本过高 |
15.某微粒的结构示意图为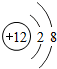 ,下列说法错误的是( )
,下列说法错误的是( )
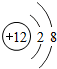 ,下列说法错误的是( )
,下列说法错误的是( )| A. | 该粒子带有两个单位的正电荷 | B. | 该粒子的原子只有两个电子层 | ||
| C. | 该粒子的原子核内有12个质子 | D. | 该粒子已经达到相对稳定结构 |
12.为确认氢氧化钠溶液与稀盐酸反应时滴加的盐酸是否过量,取少量反应后的溶液于试管中,所用的试剂及判断的方法不合理的是( )
| 实验方案 | 使用的方法或试 剂 | 判断的方法 |
| A | pH试纸 | 如果pH<7,表明盐酸已经过量 |
| B | 碳酸钠粉末 | 如果有气泡产生,表明盐酸已经过量 |
| C | 硝酸银溶液 | 如果有白色沉淀产生,表明盐酸已经过量 |
| D | 紫色石蕊溶液 | 如果溶液变成红色,表明盐酸已经过量 |
| A. | A | B. | B | C. | C | D. | D |
16.下列仪器中,不能在酒精灯火焰上直接加热的是( )
| A. | 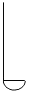 燃烧匙 | B. | 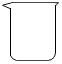 烧杯 | C. | 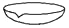 蒸发皿 | D. |  试管 |
6.消防队员用高压水枪灭火,其灭火的主要原理是( )
| A. | 隔绝空气 | B. | 清除可燃物 | ||
| C. | 降低可燃物的着火点 | D. | 使温度降到可燃物的着火点以下 |