题目内容
13.在盛有水的烧杯中加入以下某种物质,形成溶液过程中,温度上升明显,这种物质可能是( )| A. | 氯化钠 | B. | 硝酸铵 | C. | 浓硫酸 | D. | 蔗糖 |
分析 根据物质溶于水后的放热与吸热现象来考虑,要由物质溶于水的整个过程来分析
解答 解:物质溶于水分为两个过程,向水中扩散的过程吸收热量,与水分子结合形成水合分子的过程放出热量,如果吸收热量大于放出热量,就表现为吸热,如果吸收热量小于放出热量,就表现为放热,如果相等就表现为既不放热,也不吸热.
A、氯化钠溶于水溶液温度基本不变,故错误;
B、硝酸铵溶于水吸收热量,溶液温度降低,故错误;
C、浓硫酸溶于水放出热量,溶液温度升高,故正确;
D、蔗糖溶于,溶液温度基本不变,故错误;
故选:C.
点评 熟记以下物质:溶于水放热的物质有:浓硫酸、生石灰、氢氧化钠固体;溶于水吸热的有硝酸铵.

练习册系列答案
相关题目
3.因碳酸钠既能与酸反应又能与碱反应,小明和小华利用碳酸钠、稀盐酸和澄清石灰水3种试剂分别设计实验方案,探究复分解反应发生的实质.
(1)小明探究碳酸钠溶液与稀盐酸的反应
①为什么碳酸钠溶液与稀盐酸的复分解反应能够发生呢?小明认为是因为反应物中含有一些“特殊”的阴、阳离子,它们能相互结合.如上述反应中,实际参加反应的离子是CO32-和H+,而Na+、Cl-则是“旁观者”,并没有参加反应.小明得出Na+、Cl-并没有参加反应的理由是:碳酸根离子和氢离子反应生成二氧化碳和水.
②小明准备用画图的方法:在下图的圈圈中填入适当的分子或离子符号,来体现碳酸钠溶液和稀盐酸反应的实质,请你在答题卡对应的图中,与小明一起完成学习任务:
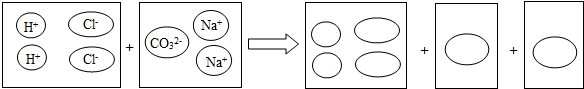
(2)小华探究碳酸钠溶液与澄清石灰水的反应
①碳酸钠溶液与澄清石灰水的反应实质是:碳酸根离子和钙离子生成碳酸钙沉淀.
②为确定碳酸钠溶液与澄清石灰水是否恰好完全反应,小华先将反应后的物质进行过滤,然后对滤液的成分提出了下列四个假设:
甲:滤液中只含氢氧化钠 乙:滤液中含氢氧化钠、氢氧化钙和碳酸钠
丙:滤液中含氢氧化钠和氢氧化钙 丁:滤液中含氢氧化钠和碳酸钠
请指出哪种假设不合理,并说明理由:乙,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠.
③接着,小华继续进行了如表探究:
老师认为小华的设计方案还不能说明碳酸钠溶液和澄清石灰水恰好完全反应,老师的评判理由是:若氢氧化钙过量与氯化钙不发生反应.
(1)小明探究碳酸钠溶液与稀盐酸的反应
①为什么碳酸钠溶液与稀盐酸的复分解反应能够发生呢?小明认为是因为反应物中含有一些“特殊”的阴、阳离子,它们能相互结合.如上述反应中,实际参加反应的离子是CO32-和H+,而Na+、Cl-则是“旁观者”,并没有参加反应.小明得出Na+、Cl-并没有参加反应的理由是:碳酸根离子和氢离子反应生成二氧化碳和水.
②小明准备用画图的方法:在下图的圈圈中填入适当的分子或离子符号,来体现碳酸钠溶液和稀盐酸反应的实质,请你在答题卡对应的图中,与小明一起完成学习任务:

(2)小华探究碳酸钠溶液与澄清石灰水的反应
①碳酸钠溶液与澄清石灰水的反应实质是:碳酸根离子和钙离子生成碳酸钙沉淀.
②为确定碳酸钠溶液与澄清石灰水是否恰好完全反应,小华先将反应后的物质进行过滤,然后对滤液的成分提出了下列四个假设:
甲:滤液中只含氢氧化钠 乙:滤液中含氢氧化钠、氢氧化钙和碳酸钠
丙:滤液中含氢氧化钠和氢氧化钙 丁:滤液中含氢氧化钠和碳酸钠
请指出哪种假设不合理,并说明理由:乙,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠.
③接着,小华继续进行了如表探究:
| 实验步骤 | 实验现象 | 结论 |
| 取少量滤液放在试管中, 再滴入氯化钙溶液 | 若生成白色沉淀 | 碳酸钠过量 |
| 若无明显现象 | 恰好反应 |
4.天然气的主要成分是( )
| A. | 甲烷 | B. | 乙烯 | C. | 一氧化碳 | D. | 氢气 |
1.下列实验现象描述正确的是( )
| A. | 铁丝在空气中燃烧,火星四射,且有黑色固体生成 | |
| B. | 红磷在空气中燃烧,产生大量烟雾 | |
| C. | 木炭在氧气中燃烧,生成黑色固体 | |
| D. | 将铁加入硫酸铜溶液中,有红色固体析出 |
5.下列“错误操作”与“可能产生的后果”不相符的是( )
| A. | 直接将水倒入装有浓硫酸的烧杯中进行稀释--烧杯受损 | |
| B. | 将滴管伸入试管中--玷污滴管 | |
| C. | 用托盘天平称取药品“左码右物”--称取较多 | |
| D. | 俯视量筒量取液体--量取较少 |
14.有3种原子,甲原子核内有6个质子和6个中子,乙原子核内有6个质子和8个中子,丙原子核内有7个质子和7个中子.下列说法正确的是( )
| A. | 甲和乙是同一种原子 | B. | 甲和乙是同一种元素 | ||
| C. | 乙和丙的核电荷数相等 | D. | 乙和丙互为同位素原子 |