题目内容
海水中有着丰富的化学资源,人们可以从海水中提取出很多的物质,如:氯化钠、镁等。下图就是利用海水提取氯化钠的大致过程:
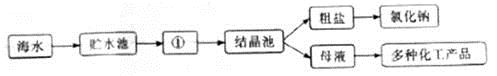
(1)图中①是 (填“蒸发池”或“冷却池”);
(2)析出晶体后的母液是氯化钠的 (填“饱和溶液”或“不饱和溶液”);
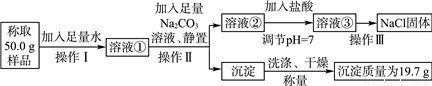
(3)实验室除去粗盐中难溶性杂质的主要实验步骤有:
Ⅰ 溶解 Ⅱ (填操作名称) Ⅲ 蒸发
上述三个步骤中,用到的同一种玻璃仪器的名称是 ,该玻璃仪器在步骤Ⅱ中的作用是 ;
(4)提取粗盐后的母液中含有较多氯化镁,从母液中提取金属镁的过程大致如下:

该过程中反应Ⅰ的基本反应类型是 ;
写出反应Ⅱ的化学方程式为 。
练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
氯化钠和碳酸钠晶体的溶解度(00C---300C)如下表所示:
00C | 100C | 200C | 300C | |
NaCl(g) | 35.7 | 35.8 | 36.0 | 36.3 |
Na2CO3·10H2O(g) | 7.0 | 12.5 | 21.5 | 38.8 |
根据上表分析下列几种说法: ①碳酸钠晶体的溶解度受温度影响较大 ②将含水各1OOg的氯化钠与碳酸钠的饱和溶液,从300C降至O0C ,析出晶体的质量相等 ③氯化钠和碳酸钠晶体的溶解度相等时所对应的温度在2O0C --300C之间 ④欲从含有少量NaCl杂质的碳酸钠浓溶液中分离出碳酸钠晶体,应采取降低溶液温度的方式上述说法中,完全正确的一组是
A. ①② B. ①③④ C. ①②③ D. ①②④


 2Fe+3CO2 D. CuO+H2
2Fe+3CO2 D. CuO+H2 Cu+H2O
Cu+H2O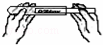 取用固体粉末
取用固体粉末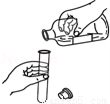 倾倒液体
倾倒液体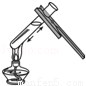 加热液体
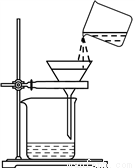
加热液体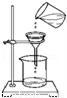 过滤
过滤