题目内容
将“神舟七号”飞船送入太空的是“长征二号”F运载火箭,火箭工作中发生的反应为C2H8N2+2R═3N2+4H2O+2CO2;下列有关说法正确的是( )
| A、R的化学式为:N4O8 |
| B、R中一定含有N,且N的化合价为+2价 |
| C、R中氧元素质量分数为:69.6% |
| D、此反应中C2H8N2与R的质量比为:60:92 |
考点:质量守恒定律及其应用,有关元素化合价的计算,元素的质量分数计算
专题:化学用语和质量守恒定律
分析:A、根据质量守恒定律的微观解释:化学反应前后原子的种类和数目不变.可知在化学反应方程式中,反应物和生成物中所含的原子的种类和数目相同.由此可推断化学反应方程式中反应物或生成物的化学式;
B、根据化合价的原则进行回答;
C、根据某元素的质量分数公式进行计算;
D、根据化学方程式中个物质的质量比进行计算.
B、根据化合价的原则进行回答;
C、根据某元素的质量分数公式进行计算;
D、根据化学方程式中个物质的质量比进行计算.
解答:解:
A、根据化学方程式C2H8N2+2R═3N2+4H2O+2CO2和质量守恒定律可得,R的化学式应含有C的个数为:(2-2)÷2=0,应含有H的个数为:(2×4-8)÷2=0,应含有N的个数为:(3×2-2)÷2=2,应含有O的个数为:(4+2×2)÷2=4.故R的化学式为:N2O4;
B、根据R的化学式为N2O4和氧元素的化合价为-2价;则根据化学式中正负化合价代数和为0,则可知N的化合价为+4价;
C、根据R的化学式为N2O4,氧元素的质量分数为
×100%≈69.6%;
D、根据化学方程式C2H8N2+2N2O4═3N2+4H2O+2CO2,此反应中C2H8N2与N2O4的质量比为:60:184.
故选:C.
A、根据化学方程式C2H8N2+2R═3N2+4H2O+2CO2和质量守恒定律可得,R的化学式应含有C的个数为:(2-2)÷2=0,应含有H的个数为:(2×4-8)÷2=0,应含有N的个数为:(3×2-2)÷2=2,应含有O的个数为:(4+2×2)÷2=4.故R的化学式为:N2O4;
B、根据R的化学式为N2O4和氧元素的化合价为-2价;则根据化学式中正负化合价代数和为0,则可知N的化合价为+4价;
C、根据R的化学式为N2O4,氧元素的质量分数为
| 16×4 |
| 14×2+16×4 |
D、根据化学方程式C2H8N2+2N2O4═3N2+4H2O+2CO2,此反应中C2H8N2与N2O4的质量比为:60:184.
故选:C.
点评:本题考查学生运用化学方程式和质量守恒定律进行计算的能力.

练习册系列答案
相关题目
下列物质的化学式中,书写错误的是( )
| A、碳酸钠 NaCO3 |
| B、氧化钙 CaO |
| C、硝酸钙 Ca(NO3)2 |
| D、硫酸锌 ZnSO4 |
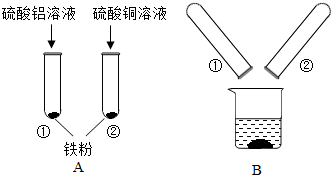
通过下列实验可以得出的结论,其中不合理的是:( )


| A、甲实验中说明水是由氢、氧两种元素组成的 |
| B、乙实验既可以说明分子在不停的运动着,又可以说明氨水显碱性 |
| C、丙实验既可以说明二氧化碳能溶于水,又可以说明二氧化碳具有酸性 |
| D、丁实验既可以说明一氧化碳具有还原性,又可以说明一氧化碳具有可燃性 |
用高铁酸钠(Na2FeO4)对河湖水消毒是城市饮水处理的新技术.已知获得高铁酸钠的反应为:Fe2O3+mNa2O2=nNa2FeO4+Na2O,下列说法中正确的是( )
| A、Na2FeO4中,铁元素的化合价+6价 |
| B、高铁酸钠中铁元素质量分数最大 |
| C、化学计量数m=n |
| D、消毒的作用是除去水中可溶性杂质 |
钠原子的结构示意图为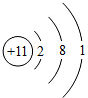 ,下列关于它的说法错误的是( )
,下列关于它的说法错误的是( )
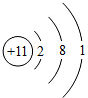 ,下列关于它的说法错误的是( )
,下列关于它的说法错误的是( )| A、钠原子的核电荷数为11 |
| B、钠原子核外共有3层电子 |
| C、钠原子易失去最外层电子 |
| D、钠原子和钠离子的化学性质相同 |
在不用指示剂的条件下,将含有盐酸的氯化钙溶液由酸性调至恰好中性,应直接向其中加入稍过量的( )
| A、Ca(OH)2溶液 |
| B、生石灰 |
| C、石灰石粉末 |
| D、纯碱 |
 金属是人类生活中的常用的材料.
金属是人类生活中的常用的材料.