题目内容
某同学用稀硫酸和氧化铜做“氧化铜+硫酸→硫酸铜+水”反应的实验,取得了下表中的数据:
根据表中的数据,请你一起来回答:
(1)哪几次实验中氧化铜有剩余?
(2)哪几次实验中硫酸有剩余?
(3)x值是多少?
(4)计算实验中所用硫酸溶液的质量分数;
(5)第2次实验中,氧化铜刚刚完全溶解时,溶液中残余硫酸的质量分数是多少?
| 实验 次数 |
氧化铜 的质量 |
硫酸溶液 的质量 |
无水硫酸 铜的产量 |
| 1 | 2.0g | 120g | 4.0g |
| 2 | 4.0g | 120g | 8.0g |
| 3 | 6.0g | 120g | 9.6g |
| 4 | 8.0g | 200g | 16.0g |
| 5 | 10.0g | 200g | x |
(1)哪几次实验中氧化铜有剩余?
(2)哪几次实验中硫酸有剩余?
(3)x值是多少?
(4)计算实验中所用硫酸溶液的质量分数;
(5)第2次实验中,氧化铜刚刚完全溶解时,溶液中残余硫酸的质量分数是多少?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:根据表中提供的数据可以判断那几次硫酸过量,那几次氧化铜过量,并且可以计算稀硫酸的质量分数及其x的值.
解答:解:由1、2、3次实验可知,第1、2次反应硫酸有剩余,第3次反应氧化铜有剩余;
第3次实验中,硫酸完全反应,设硫酸的质量为x,
CuO+H2SO4═CuSO4+H2O
98 160
x 9.6g
=
,
x=5.88g,
则稀硫酸的质量分数为:
×100%=4.9%,
根据反应的化学方程式可以计算:第4次实验中,8.0g氧化铜和200g稀硫酸恰好完全反应,生成16.0g硫酸铜;
第5次实验中,氧化铜过量,以稀硫酸计算可知,x=16.0g;
第2次实验中,氧化铜刚刚完全溶解时,溶液中残余硫酸的质量分数是多少?
120g稀硫酸中,硫酸的质量为:120g×4.9%=5.88g,
设4.0g氧化铜刚刚完全溶解时消耗硫酸的质量为y,
CuO+H2SO4═CuSO4+H2O,
80 98
4.0g y
=
,y=4.9g,
剩余硫酸的质量为:5.88g-4.9g=0.98g,
则第2次实验中,氧化铜刚刚完全溶解时,溶液中残余硫酸的质量分数为:
×100%=0.79%;
故答案为:
(1)3、5实验中氧化铜有剩余;
(2)1、2实验中硫酸有剩余;
(3)x值是16.0g;
(4)实验中所用硫酸溶液的质量分数是4.9%;
(5)第2次实验中,氧化铜刚刚完全溶解时,溶液中残余硫酸的质量分数是0.79%.
第3次实验中,硫酸完全反应,设硫酸的质量为x,
CuO+H2SO4═CuSO4+H2O
98 160
x 9.6g
| 98 |
| 160 |
| x |
| 9.6g |
x=5.88g,
则稀硫酸的质量分数为:
| 5.88g |
| 120g |
根据反应的化学方程式可以计算:第4次实验中,8.0g氧化铜和200g稀硫酸恰好完全反应,生成16.0g硫酸铜;
第5次实验中,氧化铜过量,以稀硫酸计算可知,x=16.0g;
第2次实验中,氧化铜刚刚完全溶解时,溶液中残余硫酸的质量分数是多少?
120g稀硫酸中,硫酸的质量为:120g×4.9%=5.88g,
设4.0g氧化铜刚刚完全溶解时消耗硫酸的质量为y,
CuO+H2SO4═CuSO4+H2O,
80 98
4.0g y
| 80 |
| 98 |
| 4.0g |
| y |
剩余硫酸的质量为:5.88g-4.9g=0.98g,
则第2次实验中,氧化铜刚刚完全溶解时,溶液中残余硫酸的质量分数为:
| 0.98g |
| 4.0g+120g |
故答案为:
(1)3、5实验中氧化铜有剩余;
(2)1、2实验中硫酸有剩余;
(3)x值是16.0g;
(4)实验中所用硫酸溶液的质量分数是4.9%;
(5)第2次实验中,氧化铜刚刚完全溶解时,溶液中残余硫酸的质量分数是0.79%.
点评:本题主要考查物质之间相互作用时过量、恰好完全反应时计算方面的问题,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列关于催化剂的说法正确的是( )
| A、催化剂一定加快反应速度 |
| B、在反应前后,催化剂的化学性质和质量不发生改变 |
| C、二氧化锰就是催化剂 |
| D、所有反应都需要催化剂 |
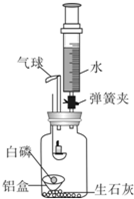 在教师的指导下,某化学兴趣小组的同学利用如图所示装置(固定装置已略去)探究燃烧等相关实验.已知,白磷的着火点40℃;该装置气密性良好,且生石灰适量、白磷过量、注射器中的水均足量.实验步骤及部分现象记录如下表.
在教师的指导下,某化学兴趣小组的同学利用如图所示装置(固定装置已略去)探究燃烧等相关实验.已知,白磷的着火点40℃;该装置气密性良好,且生石灰适量、白磷过量、注射器中的水均足量.实验步骤及部分现象记录如下表.