题目内容
12.某活动小组用废铜制取硫酸铜溶液,实验过程为:
(1)废铜在空气中加热后得到的氧化铜中含有少量铜,原因是b(填字母序号).
a.加热时氧化铜易分解生成铜
b.铜与氧气没有完全反应
c.加热时铜不能与氧气反应
(2)氧化铜与稀硫酸反应的化学方程式为CuO+H2SO4═CuSO4+H2O.
(3)盛放硫酸铜溶液不宜用铁制容器的原因是Fe+CuSO4═FeSO4+Cu(用化学方程式解释).
分析 (1)固体和气体反应会因为接触面积小而使反应不能完全进行;
(2)书写复分解反应的化学方程式时要首先判断能否反应,然后正确书写反应物和生成物的化学式,配平并注明条件;
(3)盛放硫酸铜溶液不宜用铁制容器是因为铁和硫酸铜溶液反应.
解答 解:(1)铜在空气中加热时,生成的氧化铜会覆盖在铜的表面,使铜不能和氧气接触,不能完全反应;
(2)氧化铜与稀硫酸反应生成硫酸铜和水,化学方程式为:CuO+H2SO4=CuSO4+H2O;
(3)因为铁比铜活泼,能与硫酸铜溶液反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4═FeSO4+Cu.
故答案为:(1)b;
(2)CuO+H2SO4═CuSO4+H2O;
(3)Fe+CuSO4═FeSO4+Cu.
点评 本题考查了同学们的分析能力还有书写化学方程式的能力.

练习册系列答案
相关题目
2.下列物质露置于空气中,一段时间后,质量不会增加的是( )
| A. | 浓硫酸 | B. | 氢氧化钠 | C. | 浓盐酸 | D. | 澄清石灰水 |
7.按下列实验方法操作,能达到要求的是( )
| A. | 用托盘天平称量25.20g氯化钠固体 | |
| B. | 用湿润的红色布条检验HCl气体中 是否含有Cl2 | |
| C. | 用NaOH溶液和FeCl3溶液制备Fe(OH)3胶体 | |
| D. | 将氢氧化钠固体在容量瓶中溶解,配制一定物质的量浓度的NaOH溶液 |
2.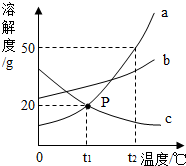 如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
 如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )| A. | a的溶解度大于b的溶解度 | |
| B. | c一定是熟石灰的溶解度曲线 | |
| C. | p点表示在t1℃,a、c两物质的饱和溶液溶质质量分数相同 | |
| D. | 三种物质的饱和溶液分别从t2℃降至t1℃,a、b析出的晶体质量相等 |
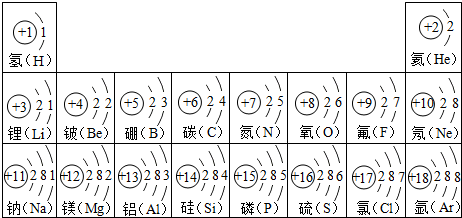
 如图是某化学学习小组设计的用一氧化碳还原氧化铜的实验装置,请回答以下问题:
如图是某化学学习小组设计的用一氧化碳还原氧化铜的实验装置,请回答以下问题: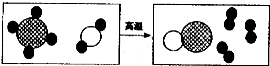
 ”表示氢分子
”表示氢分子