题目内容
煤是一种化石燃料,用煤作燃料生成的SO2气体会造成环境污染.有一种煤每燃烧1t就会释放出53.3kgSO2.如果将产生的SO2用熟石灰来完全吸收,其反应的化学方程式为:S02+Ca(OH)2═CaSO3+H20,那么燃烧5t这种煤产生的SO2在理论上需用多少千克的Ca(OH)2来吸收?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据煤的质量可以计算生成二氧化硫的质量,根据二氧化硫的质量可以计算消耗氢氧化钙的质量.
解答:解:设燃烧5t这种煤产生的SO2在理论上需用氢氧化钙的质量为x,
燃烧5t这种煤产生的二氧化硫质量为:53.3kg×5=266.5kg,
S02+Ca(OH)2═CaSO3+H20,
64 74
266.5kg x
=
,
x=308.1kg,
答:燃烧5t这种煤产生的SO2在理论上需用308.1kg的Ca(OH)2来吸收.
燃烧5t这种煤产生的二氧化硫质量为:53.3kg×5=266.5kg,
S02+Ca(OH)2═CaSO3+H20,
64 74
266.5kg x
| 64 |
| 266.5kg |
| 74 |
| x |
x=308.1kg,
答:燃烧5t这种煤产生的SO2在理论上需用308.1kg的Ca(OH)2来吸收.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
加热mg高锰酸钾制氧气,反应一段时间后停止加热,试管中残留固体wg,则生成氧气( )
| A、等于(m-w)g |
| B、大于(m-w)g |
| C、小于(m-w)g |
| D、无法确定生成O2的质量 |
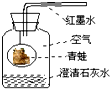 某同学为了研究动物的呼吸作用,用如图进行实验.实验过程中发现澄清石灰水变浑浊,红墨水向左移动,实验结束后,用燃着的木条放到瓶中,木条熄灭,说明动物呼吸时,消耗
某同学为了研究动物的呼吸作用,用如图进行实验.实验过程中发现澄清石灰水变浑浊,红墨水向左移动,实验结束后,用燃着的木条放到瓶中,木条熄灭,说明动物呼吸时,消耗