题目内容
11.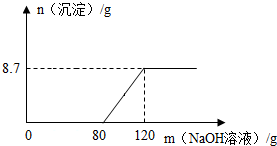 向盛有100g稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示,求
向盛有100g稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示,求(1)镁粉的质量;
(2)NaOH溶液的溶质质量分数.
分析 (1)根据Mg(OH)2中金属镁的质量即为镁粉的质量解答;
(2)根据稀硫酸和镁反应生成硫酸镁和氢气,硫酸镁和氢氧化钠反应生成氢氧化镁沉淀和硫酸钠,根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:(1)由图8可知,生成的Mg(OH)2质量为8.7g,则:
Mg(OH)2中金属镁的质量即为镁粉的质量:8.7g×$\frac{24}{\begin{array}{l}58\end{array}}$=3.6g
(2)由图8可知,与硫酸镁反应的NaOH溶液质量为120g-80g=40g
设NaOH溶液的溶质质量分数为x,则
2NaOH+MgSO4═Na2SO4+Mg(OH)2↓
2×40 58
40g×x 8.7g
$\frac{2×40}{58}$=$\frac{40g×x}{8.7g}$
x=30%
答案:
(1)镁粉的质量为3.6g;
(2)NaOH溶液的溶质质量分数为30%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
2.对于水受热变为水蒸气的现象,下列解释正确的是( )
| A. | 分子大小发生变化 | B. | 分子分成了原子 | ||
| C. | 分子之间间隙改变 | D. | 分子的数目增加 |
19.对原子核电子以及电子的运动,下列描述不正确的是( )
| A. | 原子中,电子所具有能量和运动速率几乎完全相同 | |
| B. | 电子质量很小且带负电荷 | |
| C. | 电子的运动速度接近光速 | |
| D. | 电子在原子里有“广阔”的运动空间 |
6.经过两年的化学学习,你认为下列认识正确的是( )
| A. | 化学是研究物质的组成、结构、性质和运动规律的科学 | |
| B. | 木条在空气中燃烧后质量减轻不符合质量守恒定律 | |
| C. | 食物在夏天比冬天更容易变质主要与氧气有关 | |
| D. | 要注意合理摄入人体必需元素,不足或过量均不利健康 |
16.CO2和O2是自然界中不可缺少的两种气体,它们的相同点是( )
| A. | 都是无色无味 | B. | 都能供给呼吸 | C. | 都能灭火 | D. | 都能支持燃烧 |
3.“节能减排,从我做起”.下列实验操作不符合节约原则的是( )
| A. | 甲学生用白色点滴板代替试管,进行酸、碱溶液与指示剂反应的实验 | |
| B. | 乙学生配制5%的氯化钠溶液50g,把配好的溶液装入试剂瓶盖好瓶塞,贴好标签 | |
| C. | 丙学生用氯酸钾和二氧化锰制氧气时,先点燃酒精灯,再去组装仪器 | |
| D. | 丁学生做完金属与酸的反应实验后,把多余的金属和剩余的溶液回收 |
20.下列叙述中不正确的是( )
| A. | 铁生锈后质量增加了符合质量守恒定律 | |
| B. | 镁条燃烧时,能量的变化是化学能转化为热能及光能 | |
| C. | 某有机物在空气中燃烧只生成二氧化碳和水,则该有机物一定含有碳、氢元素,可能含有氧元素 | |
| D. | 将草木灰(含K2CO3)与氯化铵混合施用,同时施加两种肥料可增加肥效 |
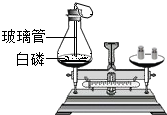 如图是小明同学利用测定白磷燃烧的实验来探究化学反应前后质量有无变化,请你回答下列问题:
如图是小明同学利用测定白磷燃烧的实验来探究化学反应前后质量有无变化,请你回答下列问题: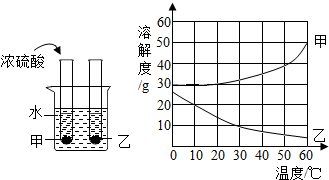 2016年我国纪念“世界水日”和“中国水周”活动的主题是“落实五大发展理念,推进最严格水资源管理”.某校化学兴趣小组进行了一系列探究小实验.
2016年我国纪念“世界水日”和“中国水周”活动的主题是“落实五大发展理念,推进最严格水资源管理”.某校化学兴趣小组进行了一系列探究小实验.