题目内容
可以将K2CO3、Ba(OH)2、BaCO3和 NaCl四种粉末一次鉴别出来的试剂是______.
【答案】分析:根据K2CO3、Ba(OH)2、BaCO3和 NaCl四种种物质的性质及变化现象的不同,分析所选试剂与四种物质发生反应时所出现的现象,利用所出现的不同现象完成四种物质的区分,化学现象一般表现为产生气体,生成沉淀、无现象.
解答:检验钡离子选用硫酸盐或硫酸产生白色沉淀,检验碳酸根离子选用酸溶液产生气泡,氯化钠和硫酸反应无明显现象,四种反应现象不同,所以选取稀硫酸溶液,稀硫酸和碳酸钾反应生成气体,和碳酸钡反应生成气体和沉淀,和氢氧化钡反应生成沉淀,和氯化钠不反应,四种现象都不同,能一次鉴别出来.
故答案为:稀硫酸(H2SO4)
点评:使用一种试剂同时鉴别多种物质,所选试剂与多种物质发生反应时,能出现多种明显不同的现象才能满足鉴别的要求.
解答:检验钡离子选用硫酸盐或硫酸产生白色沉淀,检验碳酸根离子选用酸溶液产生气泡,氯化钠和硫酸反应无明显现象,四种反应现象不同,所以选取稀硫酸溶液,稀硫酸和碳酸钾反应生成气体,和碳酸钡反应生成气体和沉淀,和氢氧化钡反应生成沉淀,和氯化钠不反应,四种现象都不同,能一次鉴别出来.
故答案为:稀硫酸(H2SO4)
点评:使用一种试剂同时鉴别多种物质,所选试剂与多种物质发生反应时,能出现多种明显不同的现象才能满足鉴别的要求.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
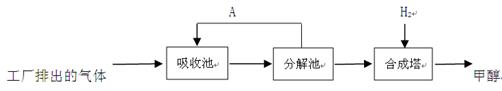
有科学家提出回收利用CO2的构想:将工厂排出的气体(含较多CO2)吹入碳酸钾溶液,从溶液中提取出CO2,又在合成塔使之变为燃料甲醇(CH3OH)。该技术流程如下:
(说明:吸收池中盛有饱和的K2CO3溶液,主要反应为:K2CO3+H2O+CO2=2KHCO3)
下列有关说法错误的是:
| A.该方法可以减少碳排放 | B.可循环利用的物质A是K2CO3 |
| C.分解池中的主要反应属于分解反应 | D.合成塔中的主要反应属于化合反应 |

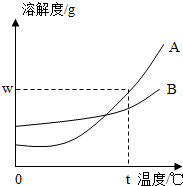 如图所示,A、B两种固体物质的溶解度曲线:
如图所示,A、B两种固体物质的溶解度曲线: