题目内容
某物质R46g在氧气中完全燃烧只生成88g的二氧化碳和54g的水.则物质R的化学式是( )
| A、CH4 |
| B、C2H2 |
| C、CH3OH |
| D、C2H5OH |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:根据质量守恒定律可知:生成二氧化碳中碳元素的质量等于该化合物中碳元素的质量;生成的水中氢元素的质量等于该化合物中氢元素的质量;其余则为氧元素的质量.根据该化合物的元素质量比就可以确定其的化学式.
解答:解:根据碳元素和氢元素守恒可知,物质R中含碳元素为:88g×
×100%=24g,氢元素的质量为:54g×
×100%=6g,则所含氧元素的质量为46g-24g-6g=16g.即该化合物是由碳元素、氢和氧元素组成的.
其中碳原子:氢原子:氧原子=
:
:
=2:6:1,
所以该物质的化学式为:C2H6O,即C2H5OH.
故选:D.
| 12 |
| 44 |
| 2 |
| 18 |
其中碳原子:氢原子:氧原子=
| 24 |
| 12 |
| 6 |
| 1 |
| 16 |
| 16 |
所以该物质的化学式为:C2H6O,即C2H5OH.
故选:D.
点评:物质在氧气中完全燃烧,产物只有二氧化碳和水.根据化学反应前后元素的种类和质量都不变,则生成的二氧化碳中碳元素的质量就是物质中碳元素的质量;生成的水中氢元素的质量就是物质中氢元素的质量.若碳元素与氢元素的质量和等于物质质量,则物质中不含氧元素;若小于物质质量,则物质中含有氧元素.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目
把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是( )
| A、硫酸钡 | B、碘 | C、硝酸铵 | D、汽油 |
某化学兴趣小组的同学开展如图所示实验.关于该实验,下列说法正确的是( )
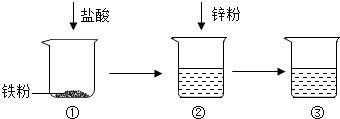

| A、②中溶液一定含有盐酸 |
| B、②中加入锌粉时一定没有气泡冒出 |
| C、③中一定没有盐酸 |
| D、③中的溶质一定没有氯化亚铁 |
“由同种元素组成的不同单质叫同素异形体”,下列各组物质属于同素异形体的是( )
| A、CO,C02 |
| B、金刚石和石墨 |
| C、02和03 |
| D、氧气和液态氮 |
关于甲乙丙三种粒子的结构示意图,下列说法正确的是( )


| A、甲是原子,乙丙是阴离子 |
| B、甲乙丙都具有相对稳定的结构 |
| C、甲乙丙属于同一种元素 |
| D、甲是稀有气体元素,乙丙是非金属元素 |
下列做法中,有益于人体健康的是( )
| A、为了杀菌和保鲜,用甲醛溶液浸泡海产品 |
| B、为了给人体补充铁元素,在酱油中加入少量铁 |
| C、为了提高牛奶的含氮量,向牛奶中添加NaN02 |
| D、为了防止污染,使用聚氯乙稀薄膜包装食品 |
推理是化学学习中常见的思维方法.下列推理正确的是( )
| A、酸能使紫色石蕊试液变红,二氧化碳也能使紫色石蕊变红,所以二氧化碳是酸 |
| B、某物质在空气中燃烧后生成二氧化碳和水,则该物质中一定含有氧元素 |
| C、向某溶液中滴加氯化钡溶液,产生不溶于稀硝酸的白色沉淀,说明该溶液中可能存在SO42- |
| D、溶液中有晶体析出,其溶质的质量减少,所以溶质的质量分数一定减小 |