题目内容
12.赤铁矿是一种常见的含铁丰富的矿石,其主要成分为氧化铁(Fe2O3).工业上常用赤铁矿来炼铁,炼铁时氧化铁中的铁元素全部变成铁单质.生铁也是一种混合物,其中含有的杂质主要为碳.请根据以上信息计算:利用含杂质10%的赤铁矿2000t,可得到含碳3%的生铁多少吨?(结果精确到0.1)分析 含杂质的物质在方程式中要转化成纯净物,因此可先求出含杂质铁矿石中三氧化二铁的质量,后根据化学方程式的计算求生成铁的质量,列综合算式时应注意含杂质与纯净物之间的关系.
解答 解:2000t矿石中含氧化铁的质量为:2000t×(1-10%)=1800t
设1600t氧化铁理论上可炼出铁的质量为x
Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
1800t x
$\frac{160}{1800t}=\frac{112}{x}$
x=1260t
折合为含杂质3%的生铁的质量为:1260t÷(1-3%)≈1299.0t
答案:可得到含杂质3%的生铁为1299.0t.
点评 此题重点考查了含杂质物质的根据化学方程式的计算,涉及到纯净物与混合物的换算,牢记利用方程式计算时“必将纯量代方程”.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.2016年某市着力打造生态旅游区,下列做法不符合这一主题的是( )
| A. |  爱护花草树木 | B. |  随意排放废水 | C. |  分类回收垃圾 | D. |  绿色低碳出行 |
20.下列物质的用途,只利用物质的物理性质的是( )
| A. | 用氧气抢救危重病人 | B. | 用氦气填充探空气球 | ||
| C. | 用氮气做保护气填充食品包装袋 | D. | 稀有气体通电发出各色的光 |
4.人类的第二杀手---心脑血管疾病,给人们的身心健康造成极大的危害.这类疾病患者大多属于酸性体质,应经常食用碱性食品.根据以表中的信息,这类患者应经常食用的食物为( )
| 食 物 | 苹 果 | 牛 奶 | 豆 制 品 | 葡 萄 |
| PH | 2.9-3.3 | 6.3-6.6 | 7.4-7.9 | 3.5-4.5 |
| A. | 牛 奶 | B. | 豆 制 品 | C. | 苹 果 | D. | 葡 萄 |
1.工业用盐主要成分亚硝酸钠,有咸味,外观与氯化钠相似,亚硝酸钠的水溶液呈碱性.日本大地震发生后,福岛第一核电站放射性物质泄漏,导致社会上曾发生不必要的“食盐恐慌”,为防止一些不法奸商用具有毒性的亚硝酸钠欺骗顾客.下列能用来区别NaNO2与NaCl固体的方法是( )
| A. | 观察颜色 | B. | 品尝味道 | ||
| C. | 用水溶解 | D. | 分别溶于水测其pH |
4.下列各组离子可在同一溶液中大量共存的是( )
| A. | H+ SO42- K+ CO32- | B. | Mg2+ Cl- OH- Na+ | ||
| C. | Fe3+ SO42- H+ Cl- | D. | Na+Ba2+ NO3-SO42- |
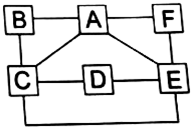 有A、B、C、D、E、F六种物质,它们间的相互关系如右图所示(连线表示能相互反应或与其溶液间能反应).己知D是一种金属单质,它可能是铝或铜;A、B、C、E、F分别是:硝酸银、生石灰、盐酸、碳酸钾、氯化钙五种物质中的某一种.其中A和C反应时生成一种无色气体.
有A、B、C、D、E、F六种物质,它们间的相互关系如右图所示(连线表示能相互反应或与其溶液间能反应).己知D是一种金属单质,它可能是铝或铜;A、B、C、E、F分别是:硝酸银、生石灰、盐酸、碳酸钾、氯化钙五种物质中的某一种.其中A和C反应时生成一种无色气体.