题目内容
1.将铁片分别插入稀硫酸、氯化镁、硝酸铜溶液中,反应后将铁片取出干燥后称量,金属片质量增加的是硝酸铜;溶液质量变大的是稀硫酸;有气泡产生的反应的化学方程式是Fe+H2SO4=FeSO4+H2↑.分析 根据金属活动性顺序可知,排在氢前面的金属会与酸反应生成氢气,排在前面的金属会将排在后面的金属从其盐溶液中置换出来进行分析.
解答 解:在金属活动性顺序中,铁排在镁之后,不会与氯化镁反应,每56份质量的铁和98份质量的硫酸反应会生成152份质量的硫酸亚铁和2份质量的氢气,每56份质量的铁和硝酸铜反应会置换出64份质量的铜,所以反应后将铁片取出干燥后称量,金属片质量增加的是硝酸铜;溶液质量变大的是稀硫酸;有气泡产生的反应的化学方程式是:Fe+H2SO4=FeSO4+H2↑.
故答案为:硝酸铜,稀硫酸,Fe+H2SO4=FeSO4+H2↑.
点评 本题考查了金属与酸以及与盐之间反应的质量的计算,完成此题,可以依据金属活动性顺序及其意义并结合反应前后物质的质量关系进行.

练习册系列答案
相关题目
9.日常生活中的下列变化属于化学变化的是( )
| A. | 汽油挥发 | B. | 电灯发光 | C. | 车胎爆炸 | D. | 粮食酿酒 |
10.下列变化属于化学变化的是( )
| A. | 汽油挥发 | B. | 灯泡发光 | C. | 燃放烟火 | D. | 冰雪融化 |
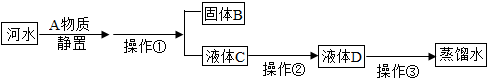

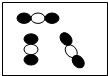
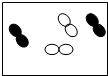
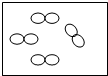

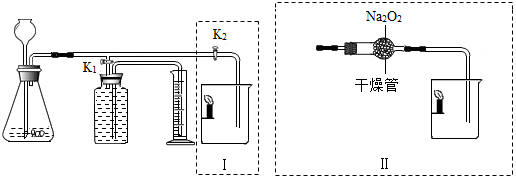
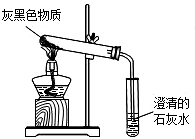 镁将成为21世纪重要的轻型环保材料,我国含有非常丰富的镁资源.
镁将成为21世纪重要的轻型环保材料,我国含有非常丰富的镁资源.