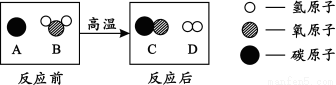
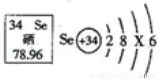
题目内容
(8分)科技节活动中,化学实验小组做了如下实验,请回答以下问题。
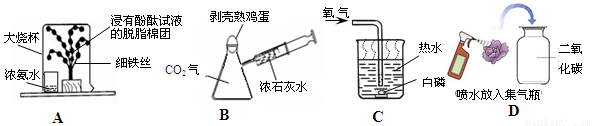
(1)图A所示实验可观察到“铁树”上浸有无色酚酞试液的棉团由白色变为 色,该实验中没有涉及的性质是 (填字母)。
A.氨分子是不断运动的 B.氨分子有一定质量 C.浓氨水具有挥发性
(2)图C所示实验发生反应的化学方程式为 。
(3)图C所示实验中,当通过导管向热水中通入氧气时,白磷在水下燃烧,该实验说明燃烧需要的条件为:①可燃物;②达到燃烧所需要的 ;③ 。
(4)图D所示实验观察到紫色小花变为红色,小花变红的原因是
(用化学方程式表示)。
(1)红 B (2)4P + 5O2 点燃 2P2O5 (3)温度 与氧气接触
(4)CO2 + H2O === H2CO3
【解析】
试题分析:(1)浓氨水显碱性,能使无色酚酞溶液变红,故图A所示实验可观察到“铁树”上浸有无色酚酞试液的棉团由白色变为色红,原因是浓氨水具有挥发性,氨气分子不断运动到浸有无色酚酞试液的棉团上,故该实验中没有涉及的性质:氨分子有一定质量,选B
(2)图C所示实验发生反应是红磷燃烧,化学方程式为:4P + 5O2 点燃 2P2O5
(3)燃烧需要的三个条件为:①可燃物;②达到燃烧所需要的温度;③与氧气接触
(4)图D所示实验观察到紫色小花变为红色,小花变红的原因是二氧化碳与水反应生成了碳酸,化学方程式为:CO2 + H2O === H2CO3
考点:分子的基本性质,燃烧的条件,二氧化碳的化学性质

(7分)(1)小方用下图所示装置对二氧化碳的灭火实验进行研究,
实验的结论是______________________________________。
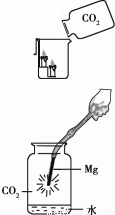
(2)【提出问题】二氧化碳能否支持燃烧?
【猜想假设】镁能在二氧化碳中燃烧。
【查阅资料】①氧化镁、氢氧化镁均是白色难溶于水的固体
②MgO+2HCl= MgCl2+H2O
③MgCl2+2NaOH=Mg(OH)2↓+2NaCl
【实验探究】
①上图中镁带剧烈燃烧,冒白烟,有黑色固体生成,并放出大量的热。
②为检验生成物的成分,做如下实验。
实验步骤 | 实验现象 | 实验结论和 化学方程式 | |
向广口瓶中加入过量盐酸,充分反应后过滤,在滤纸上留有黑色固体。 | I、将黑色固体收集、洗涤、干燥后,点燃,在火焰上方罩一个蘸有澄清石灰水的烧杯。 | 黑色固体燃烧,烧杯内壁出现白色浑浊。 | 黑色固体是 ; 涉及该步骤反应的化学方程式: 。 |
II、取少量滤液于试管中,逐滴加入氢氧化钠溶液。 | 有白色沉淀产生。 | 白烟的成分是 。 | |
③为了回收II中的白色沉淀,证明沉淀完全的实验方法是 。
(要求写出步骤、试剂、现象和结论)。
【反思提高】通过此次实验的探究,你对燃烧的条件或二氧化碳的灭火有何新认识 。
(7分)溶液是生产生活中常见的物质,依据相关信息回答问题:
资料:硝酸钾的溶解度数据(部分数据已做取整数处理)如下表所示:
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
溶解度/g | 21 | 32 | 46 | 64 | 86 | 110 | 138 |
(1)农业上,硝酸钾用作水溶性肥料,为作物补充氮和钾元素。硝酸钾溶液中的溶质是______。
(2)A、B、C、D四个烧杯中分别盛有100g水,在40℃时,向四个烧杯中分别加入110g、86g、64g、32g硝酸钾,充分溶解,如图所示。

①(填字母序号) 中盛的一定是饱和溶液。
②使B烧杯的溶液升温至50℃时,溶液的质量为 g。
③采用一种方法使A中的固体恰好溶解。对于最终四个烧杯中的溶液,下列说法正确的是 (填字母序号)。
a.溶剂质量可能相等
b.溶质质量可能相等
c.溶质质量分数可能有相等的
d.烧杯A中的溶液质量分数可能最大
(3)工业上利用电解饱和氯化钠溶液可制得重要化工产品氢氧化钠。氢氧化钠溶液可用于治理含二氧化硫的废气并回收二氧化硫,反应的主要流程如下:
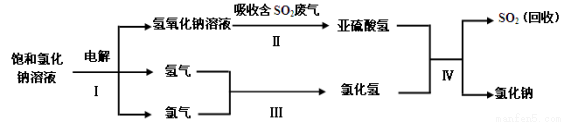
①实际生产中,在一定温度下,配制100t溶质的质量分数为25%的饱和氯化钠溶液,需水的质量为 t。
②以上流程中,可循环使用的物质是 。
③亚硫酸氢钠(NaHSO3)中硫元素的质量分数为 %(计算结果精确到0.1%)。