题目内容
7.写出下列符号中数字“3”的意义(1)O31个臭氧分子中含有3个氧原子(2)3K钾原子的个数为3(3)Al3+一个铝离子带有3个单位的正电荷.
分析 (1)标在化学式中元素右下角的数字表示一个分子中所含原子的数目.
(2)标在元素符号前面的数字表示原子的个数.
(3)标在元素符号右上角的数字表示离子所带电荷数.
解答 解:(1)标在化学式中元素右下角的数字表示一个分子中所含原子的数目,O3中的“3”表示1个臭氧分子中含有3个氧原子.
(2)标在元素符号前面的数字表示原子的个数,3K中的“3”表示钾原子的个数为3.
(3)标在元素符号右上角的数字表示离子所带电荷数,Al3+中的“3”表示一个铝离子带有3个单位的正电荷.
故答案为:(1)1个臭氧分子中含有3个氧原子;(2)钾原子的个数为3;(3)一个铝离子带有3个单位的正电荷.
点评 本题难度不大,主要考查了元素符号不同位置的数字表示的意义,掌握标在元素符号不同位置的数字所表示的意义是正确解答此类题的关键所在.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
18.我国青海湖采集的天然碱样品可表示为aNa2CO3•bNaHCO3•cH2O(a、b、c为最简整数比).小红同学为测定其组成,称取该天然碱样品16.6g进行如下实验:
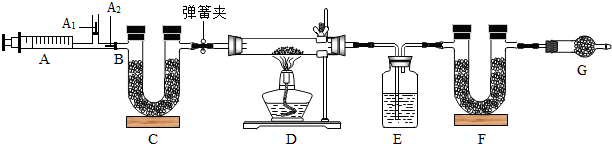
已知:①碳酸钠比较稳定,加热时不分解;②图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭.
(一)实验步骤 ①组装好装置,检查气密性②反复推拉注射器③称量E、F的质量④关闭弹簧夹,加热D处试管直到反应不再进行⑤打开弹簧夹,再次反复缓缓推拉注射器⑥再次称量E、F的质量.
(二)问题探究:
(1)E中的药品为浓硫酸,E的作用是吸收水蒸气.C、F、G中装有碱石灰(CaO与NaOH的固体混合物),则C的作用是除去空气中的二氧化碳,F的作用是吸收生成的二氧化碳,G的作用是防止空气的二氧化碳和水蒸气进入F装置.
(2)实验步骤②与③能否颠倒不能(填“能”或“不能”).若不进行步骤⑤的操作,则所测得的碳酸氢钠质量分数偏小(填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是使反应生成的水蒸气和二氧化碳被充分吸收.
(3)据表,16.6g天然碱中结晶水的质量为1.8g,Na2CO3的质量为10.6g,该天然碱的化学式中a:b:c=2:1:2.

已知:①碳酸钠比较稳定,加热时不分解;②图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭.
(一)实验步骤 ①组装好装置,检查气密性②反复推拉注射器③称量E、F的质量④关闭弹簧夹,加热D处试管直到反应不再进行⑤打开弹簧夹,再次反复缓缓推拉注射器⑥再次称量E、F的质量.
(二)问题探究:
(1)E中的药品为浓硫酸,E的作用是吸收水蒸气.C、F、G中装有碱石灰(CaO与NaOH的固体混合物),则C的作用是除去空气中的二氧化碳,F的作用是吸收生成的二氧化碳,G的作用是防止空气的二氧化碳和水蒸气进入F装置.
(2)实验步骤②与③能否颠倒不能(填“能”或“不能”).若不进行步骤⑤的操作,则所测得的碳酸氢钠质量分数偏小(填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是使反应生成的水蒸气和二氧化碳被充分吸收.
| 反应前 | 反应后 |
| E的质量为100.0g | E的质量为102.25g |
| F的质量为50.0g | F的质量为51.1g |
2.下列是四位同学实验时记录的实验数据和实验现象,其中正确的是( )
| A. | 小明用10mL量筒量取了8.25mL的稀硫酸 | |
| B. | 小华用托盘天平秤量了13.64g的固体锌粒 | |
| C. | 小雨将点燃的金属钠放进氯气瓶中,生成氯化钠 | |
| D. | 小芳将食盐放水中,搅拌后实验逐渐溶解了 |
19.下列过程涉及到的变化主要是化学变化的是 ( )
| A. | 氢气燃烧 | B. | 石油分馏 | C. | 榨取果汁 | D. | 冰雪融化 |
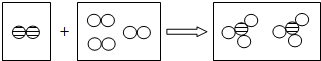
16.如图是某化学反应的微观模型,“○”、“ ”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
 ”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
| A. | 该反应属于分解反应 | B. | 反应物和生成物中只有一种单质 | ||
| C. | 反应前后元素的种类发生了变化 | D. | 反应中共有两种元素参与 |
17.下列不属于氧气的用途的是 ( )
| A. | 急救 | B. | 气焊 | C. | 潜水 | D. | 灭火 |