题目内容
3.学习化学的一个重要途径是科学探究,实验是科学探究的重要手段,下列化学实验操作不正确的是( )| A. |  液体的倾倒 | B. |  液体的量取 | C. | 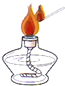 点燃酒精灯 | D. | 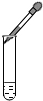 滴加液体 |
分析 A、液体药品的取用,注意试剂瓶盖的放置、标签的位置;
B、量筒的使用:注意视线与液面的关系;
C、酒精灯的注意事项进行解答;
D、使用胶头滴管滴加少量液体的操作,注意胶头滴管的位置是否伸入到试管内.
解答 解:A、液体药品的取用时,试剂瓶盖要倒放桌面上,标签向着手心.操作正确;
B、量筒的使用时,量筒放在桌面上,视线与液体的凹液面最低处保持水平.操作正确.
C、酒精灯用火柴点燃,不能用燃着的酒精灯引燃,操作正确.
D、胶头滴管应竖直向下且不能伸入试管,伸入试管会造成胶头滴管污染,进而污染药品污染.操作错误.
故选D.
点评 本题主要考查固体和液体药品的取用,以及量筒的使用及其注意事项.根据操作要求可以判断操作是否符合实验室的规定.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案
相关题目
14. 在新能源汽车未普及时,如图所示为一种“节能减排”的有效措施.以下对乙醇作汽车燃料的描述错误的是( )
在新能源汽车未普及时,如图所示为一种“节能减排”的有效措施.以下对乙醇作汽车燃料的描述错误的是( )
 在新能源汽车未普及时,如图所示为一种“节能减排”的有效措施.以下对乙醇作汽车燃料的描述错误的是( )
在新能源汽车未普及时,如图所示为一种“节能减排”的有效措施.以下对乙醇作汽车燃料的描述错误的是( )| A. | 原料来源丰富 | |
| B. | 是可再生能源 | |
| C. | 燃烧完全没有污染 | |
| D. | 乙醇是以高粱、玉米等为原料制得的 |
11.下列物质属于纯净物的是( )
| A. | 冰水混合物 | B. | 清澈的泉水 | C. | 清新的空气 | D. | 澄清石灰水 |
15.雯雯在自学碳酸钠性质时,查到了以下资料:
①CO2+Na2CO3+H2O═2NaHCO3,CO2通入饱和碳酸钠溶液会产生白色沉淀,CO2不溶于饱和碳酸氢钠溶液.
②碳酸钠、碳酸氢钠在不同温度下的溶解度
【进行实验1】验证CO2通入饱和碳酸钠溶液会产生白色沉淀
①配制碳酸钠溶液:取100g 20℃的水,加入35g碳酸钠固体,搅拌后,静置,取上层清液.
②利用装置一进行实验,连续5分钟向新制得的碳酸钠溶液中通入CO2.
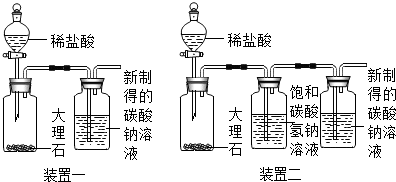
【发现问题】实验中,始终没有看到沉淀现象,原因是什么呢?雯雯进行了以下实验探究.
【进行实验2】
(1)在0℃~30℃,Na2CO3和NaHCO3的溶解度受温度变化影响较大的是碳酸钠.
(2)大理石与稀盐酸反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)装置二中饱和碳酸氢钠溶液的作用是吸收氯化氢气体,从而排除氯化氢气体对实验的干扰.
【进行实验3】
(4)雯雯在最初的实验中没有看到沉淀现象的原因是配制的碳酸钠溶液没有达到饱和.
(5)CO2通入饱和碳酸钠溶液会产生白色沉淀的原因是碳酸氢钠溶解度小于碳酸钠,水减少,生成的碳酸氢钠的质量大于反应的碳酸钠.
(6)请你依据题中信息,写出一种能够区分碳酸钠和碳酸氢钠固体的实验方案.
①CO2+Na2CO3+H2O═2NaHCO3,CO2通入饱和碳酸钠溶液会产生白色沉淀,CO2不溶于饱和碳酸氢钠溶液.
②碳酸钠、碳酸氢钠在不同温度下的溶解度
| 0℃ | 10℃ | 20℃ | 30℃ | |
| Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 |
①配制碳酸钠溶液:取100g 20℃的水,加入35g碳酸钠固体,搅拌后,静置,取上层清液.
②利用装置一进行实验,连续5分钟向新制得的碳酸钠溶液中通入CO2.

【发现问题】实验中,始终没有看到沉淀现象,原因是什么呢?雯雯进行了以下实验探究.
【进行实验2】
| 实验操作 | 实验现象 |
| ①取100g 20℃的水,加入35g碳酸钠固体,搅拌后,静置,取上层清液 ②利用装置二进行实验,连续5分钟向新制得的碳酸钠溶液中通入CO2 | 没有出现白色沉淀 |
(2)大理石与稀盐酸反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)装置二中饱和碳酸氢钠溶液的作用是吸收氯化氢气体,从而排除氯化氢气体对实验的干扰.
【进行实验3】
| 实验操作 | 实验现象 |
| ①取100g热开水,加入35g碳酸钠固体,完全溶解,再降温至20℃,取上层清液 ②利用装置一和装置二分别进行实验,连续3分钟向新制得的碳酸钠溶液中通入CO2 | 装置一和装置二中的碳酸钠溶液中均出现白色沉淀 |
(5)CO2通入饱和碳酸钠溶液会产生白色沉淀的原因是碳酸氢钠溶解度小于碳酸钠,水减少,生成的碳酸氢钠的质量大于反应的碳酸钠.
(6)请你依据题中信息,写出一种能够区分碳酸钠和碳酸氢钠固体的实验方案.
12.下列各组物质按单质、氧化物、混合物的顺序排列的是( )
| A. | 冰、干冰、赤铁矿 | B. | 氢气、生石灰、煤 | ||
| C. | 红磷、纯碱、石油 | D. | 金刚石、熟石灰、空气 |