题目内容
17.实验室需配制10%的稀硫酸200g,需要溶质质量分数为98%;密度是1.84g.mL-1的浓硫酸多少毫升?加多少毫升水?(水的密度是1g.mL-1)分析 溶液稀释前后,溶质质量不变.
解答 解:设需要浓硫酸的体积为V,根据稀硫酸和浓硫酸中溶质的质量不变,可以列出如下关系:
200g×10%═98%×1.84 g.mL-1×V,
V═11.1mL,
需加水的质量为:200g-200g×10%÷98%=179.6g,
需加水的体积=179.6g÷1g.mL-1=179.6mL,
答:需要98%浓硫酸的体积为11.1mL,需加水的体积为179.6mL.
点评 本题是借助于数学模型,利用公式来分析和解决化学计算中的有关问题,要求学生有较强的数据分析能力.

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
7.下列有关原子的叙述中,正确的是( )
| A. | 任何物质都是由原子构成的 | |
| B. | 原子都是由质子和电子构成的 | |
| C. | 原子都是由原子核和核外电子构成的 | |
| D. | 原子中质子数等于中子数 |
12.下列化学反应中能产生吸热现象的是( )
| A. | 镁条与稀盐酸反应 | B. | 分解高锰酸钾制氧气 | ||
| C. | 催化分解双氧水制取氧气 | D. | 木炭燃烧生成一氧化碳 |
9.二氧化碳的捕捉与封存是实现温室气体减排的重要途径之一,科学家利用NaOH溶液喷淋“捕捉”空气中的CO2(如图).则关于该方法的叙述正确的是( )
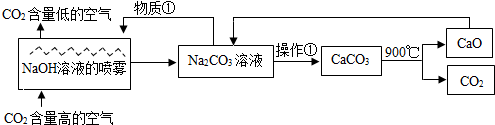

| A. | 该方法中包含复分解反应、分解反应、置换反应等 | |
| B. | 整个过程至少有2种物质可以循环利用 | |
| C. | 操作①是蒸发浓缩、降温结晶 | |
| D. | 物质①是NaOH溶液 |
6.化肥对提高粮食产量有重要作用.下列化肥中属于复合肥料的是( )
| A. | CO(NH2)2 | B. | KNO3 | C. | NH4Cl | D. | Ca3(PO4)2 |
7.做中和反应实验时,我将稀盐酸滴入氢氧化钠溶液中,意外看到有气泡产生.小伟提醒:是不是拿错了药品?我查验后确认药品没错,只是在瓶口发现有白色粉末状物质.我认为是氢氧化钠溶液变质了.
(1)氢氧化钠溶液变质的原因是CO2+2NaOH═Na2CO3+H2O.
(2)利用与上述实验不同的方法,我又设计了一个实验再次确认该氢氧化钠溶液已变质.
(3)该氢氧化钠溶液是部分变质还是全部变质?
写出(3)中所涉及到的一个化学方程式Na2CO3+BaCl2═2NaCl+BaCO3↓.
(1)氢氧化钠溶液变质的原因是CO2+2NaOH═Na2CO3+H2O.
(2)利用与上述实验不同的方法,我又设计了一个实验再次确认该氢氧化钠溶液已变质.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量氢氧化钠溶液于试管中,滴加稀盐酸 | 有气泡产生 | 该氢氧化钠溶液已变质 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量样品于试管中,加入足量的BaCl2溶液,静置在上层清液滴加几滴无色酚酞试液 | 白色沉淀,液体变红 | 该氢氧化钠溶液部分已变质 |