题目内容
已知反应2A+B═2C+D,若反应前A和B的混合物的质量为20g,充分反应后B剩余2g,生成8gC,则C与D的相对分子质量之比是( )
| A、4:5 | B、2:5 |
| C、5:4 | D、5:2 |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:掌握质量守恒定律的内容:在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.
解答:解:根据题意可知,反应物A和B的质量总和为20g-2g=18g;
根据质量守恒定律得:生成D的质量为18g-8g=10g;
因此,反应生成的C与D的质量比:8g:10g.
设C的相对分子质量为x,D的相对分子质量为y,
2A+B═2C+D
8g 10g
2x y
=
=
故选B.
根据质量守恒定律得:生成D的质量为18g-8g=10g;
因此,反应生成的C与D的质量比:8g:10g.
设C的相对分子质量为x,D的相对分子质量为y,
2A+B═2C+D
8g 10g
2x y
| 8g |
| 10g |
| 2x |
| y |
| x |
| y |
| 2 |
| 5 |
故选B.
点评:该题考查的是质量守恒定律及化学方程式的计算,解答时首先分析出反应物与生成物,找准“参加”或“生成”的物质质量,利用物质质量比或质量守恒定律进行计算即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在今年6月云南普洱地震后的救援行动中,为了搜索埋在废墟中的幸存者,人们用了搜救犬,搜救犬能根据人体发出的气味发现幸存者.试用化学观点从微粒的角度分析能发现幸存者的原因是( )
| A、分子很小 |
| B、分子在不停地运动 |
| C、分子间有间隙 |
| D、分子是由原子构成 |
下列各组物质的鉴别方法正确的是
| 待鉴别的物质 | 鉴别方法 | |
| A | 硬水、软水 | 加肥皂水、搅拌、观察现象 |
| B | 氧化铜、四氧化三铁 | 观察颜色 |
| C | N2、CO2 | 分别伸入燃着的木条,观察现象 |
| D | O2、CO2 | 分别伸入燃着的木条,观察现象 |
下列含氯元素的物质中,氯元素的化合价为-1价的是( )
| A、Cl2 |
| B、KClO3 |
| C、HCl |
| D、HClO |
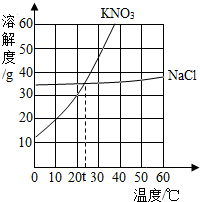 如图为硝酸钾和氯化钠两物质的溶解度曲线,回答下列问题:
如图为硝酸钾和氯化钠两物质的溶解度曲线,回答下列问题: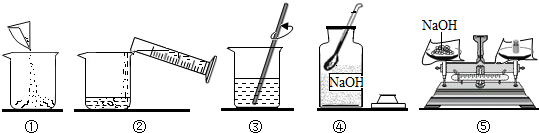
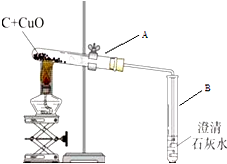 化学教材设计的木炭还原氧化铜试验的装置如图,按要求回答下列问题:
化学教材设计的木炭还原氧化铜试验的装置如图,按要求回答下列问题: