题目内容
1.根据要求写出下列反应的化学方程式.(1)“曾青得铁则化为铜”反应原理的化学方程式为Fe+CuSO4═FeSO4+Cu;
(2)稀盐酸除铁锈反应的化学方程式为6HCl+Fe2O3═2FeCl3+3H2O;
(3)用熟石灰和纯碱制烧碱反应原理的化学方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,该反应的基本类型是复分解反应.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答 解:(1)“曾青得铁则化为铜”反应原理的化学方程式为Fe+CuSO4═FeSO4+Cu;
(2)稀盐酸除铁锈反应的化学方程式为6HCl+Fe2O3═2FeCl3+3H2O;
(3)用熟石灰和纯碱制烧碱反应原理的化学方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,该反应的基本类型复分解反应;
故答案为:(1)Fe+CuSO4═FeSO4+Cu或Fe+CuCl2═FeCl2+Cu或Fe+Cu(NO3)2═Fe(NO3)2+Cu;(2)6HCl+Fe2O3═2FeCl3+3H2O;(3)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH; 复分解反应
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列家庭小实验能成功的是( )
| A. | 用淬火处理后的缝衣钢针制钓鱼钩 | B. | 用食盐水除去热水瓶中的水垢 | ||
| C. | 用电池“锌皮”与食醋反应制氢气 | D. | 用加热的方法修补电木插座 |
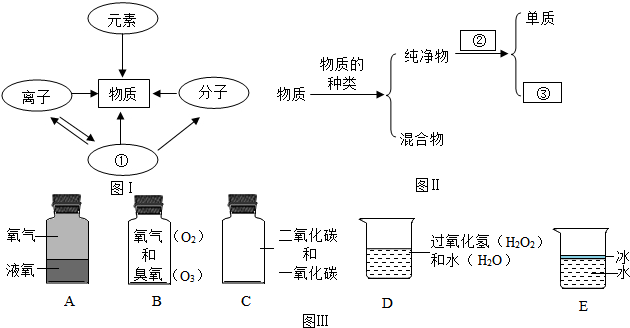
12.已知O2与O3是氧元素的两种不同单质,常温下单质硫主要以S8形式存在.加热时,S8会转化为S6、S4、S2等.当温度达到750℃时,硫蒸气主要以S2形式存在(占92%).下列说法中正确的是( )
| A. | S8转化为S6、S4、S2属于物理变化 | |
| B. | 不论哪种硫分子,完全燃烧时都生成SO2 | |
| C. | 常温条件下单质硫不存在分子 | |
| D. | 把硫单质在空气中加热到750℃即得S2 |
6.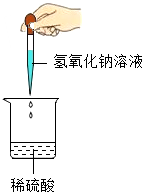 某学习小组的同学在做氢氧化钠溶液与稀硫酸的中和反应实验时(如下图所示),忽然发现没有加入指示剂.于是将实验改为探究烧杯内溶液中溶质的成分.
某学习小组的同学在做氢氧化钠溶液与稀硫酸的中和反应实验时(如下图所示),忽然发现没有加入指示剂.于是将实验改为探究烧杯内溶液中溶质的成分.
【提出问题】烧杯内的溶液中溶质是什么?
【猜想】同学们经过讨论,一致认为溶质一定有硫酸钠,写出该反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O;
除硫酸钠以外,小明同学认为还可能有氢氧化钠,小丽同学认为还可能有硫酸.
【查阅资料】硫酸钠溶液呈中性.
【设计与实验】
(1)取少量烧杯中溶液于试管中,滴加酚酞试液,无明显现象,据此推断小明同学的猜想不成立,理由是酚酞试液没有变红,溶液中没有氢氧化钠;
(2)取少量烧杯中溶液于试管中,滴加氯化钡溶液,有白色沉淀生成,据此确定溶质还有硫酸.反应的化学方程式为BaCl2+H2SO4═BaSO4↓+2HCl;
(3)小芳同学提出质疑,因为溶液中硫酸钠与氯化钡反应也会产生白色沉淀,为了证明溶质是否还有硫酸,请你与同学们一起进行如下探究(要求不选指示剂和pH试纸).
【评价与反思】在探究化学反应后的剩余物质的成分时,除了考虑生成物外,还要考虑反应物的用量.
 某学习小组的同学在做氢氧化钠溶液与稀硫酸的中和反应实验时(如下图所示),忽然发现没有加入指示剂.于是将实验改为探究烧杯内溶液中溶质的成分.
某学习小组的同学在做氢氧化钠溶液与稀硫酸的中和反应实验时(如下图所示),忽然发现没有加入指示剂.于是将实验改为探究烧杯内溶液中溶质的成分.【提出问题】烧杯内的溶液中溶质是什么?
【猜想】同学们经过讨论,一致认为溶质一定有硫酸钠,写出该反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O;
除硫酸钠以外,小明同学认为还可能有氢氧化钠,小丽同学认为还可能有硫酸.
【查阅资料】硫酸钠溶液呈中性.
【设计与实验】
(1)取少量烧杯中溶液于试管中,滴加酚酞试液,无明显现象,据此推断小明同学的猜想不成立,理由是酚酞试液没有变红,溶液中没有氢氧化钠;
(2)取少量烧杯中溶液于试管中,滴加氯化钡溶液,有白色沉淀生成,据此确定溶质还有硫酸.反应的化学方程式为BaCl2+H2SO4═BaSO4↓+2HCl;
(3)小芳同学提出质疑,因为溶液中硫酸钠与氯化钡反应也会产生白色沉淀,为了证明溶质是否还有硫酸,请你与同学们一起进行如下探究(要求不选指示剂和pH试纸).
| 实验步骤 | 实验现象 | 实验结论与解释 |
| 取少量烧杯中溶液于试管中,加入锌(填试剂名称) | 有气泡产生 | 溶质还有硫酸反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑ |
13.2008年北京奥运会的理念是“绿色奥运、科技奥运、人文奥运”,在激动人心的体育世界中,处处充满这化学知识.请回答:
(1)自第十一届奥运会以来,历届开幕式都要举行颇为隆重的“火炬接力”.奥运“祥云”火炬的燃料成分中含有液态丙烷,请通过比较在下表中写出丙烷的化学式C3H8.
(2)发令枪响后为什么会产生白烟呢?火药纸里的药粉含有氯酸钾和红磷,扣动扳机时,发生了如下化学反应:①氯酸钾受撞击分解产生氧气:2KClO3$\stackrel{撞击}{=}$2KCl+3O2↑;
②4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5(用化学方程式表示),产生大量白烟.
(3)我们常看到队医用一个小喷壶,在运动员受伤的部位喷了几下,然后受伤的运动员竟又生龙活虎地冲向了球场.小壶里装的是氯乙烷(CH3CH2Cl),一种无色、沸点只有13.1℃的易挥发有机物.当氯乙烷药液喷洒在运动员受伤部位时,很快会“消失”,这说明(填分子的一种基本性质)分子是不断运动着.由于氯乙烷挥发吸热(填“吸热”或“放热”)使皮肤表面的温度骤然下降,知觉减退,从而起到镇痛和局部麻醉的独特作用.
(1)自第十一届奥运会以来,历届开幕式都要举行颇为隆重的“火炬接力”.奥运“祥云”火炬的燃料成分中含有液态丙烷,请通过比较在下表中写出丙烷的化学式C3H8.
| 物质 | 甲烷 | 乙烷 | 丙烷 | 丁烷 | 戊烷 | 己烷 |
| 化学式 | CH4 | C2H6 | C3H8 | C4H10 | C5H12 | C6H14 |
②4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5(用化学方程式表示),产生大量白烟.
(3)我们常看到队医用一个小喷壶,在运动员受伤的部位喷了几下,然后受伤的运动员竟又生龙活虎地冲向了球场.小壶里装的是氯乙烷(CH3CH2Cl),一种无色、沸点只有13.1℃的易挥发有机物.当氯乙烷药液喷洒在运动员受伤部位时,很快会“消失”,这说明(填分子的一种基本性质)分子是不断运动着.由于氯乙烷挥发吸热(填“吸热”或“放热”)使皮肤表面的温度骤然下降,知觉减退,从而起到镇痛和局部麻醉的独特作用.
10.请仿照示例在“判断与解释”栏中回答有关问题.
| 理解与建构 | 判断与解释 |
| 例:所有的原子核内都有质子、中子. | 不正确,如:H的原子核内没有中子 |
| 练1:物质与氧气发生的氧化反应都是化合反应. | |
| 练2:中和反应生成盐和水,则生成盐和水的反应都是中和反应. | |
| 练3:一种单质中只含一种元素,一种混合物中至少含有两种元素. | |
| 练4:在空气中完全燃烧生成CO2和H2O的化合物,其组成中只含有C、H两种元素. |
11.下列叙述正确的是( )
| A. | 对人体健康而言,铅、镉、汞等是有害元素 | |
| B. | 钙、铁、锌都是人体必需的微量元素 | |
| C. | 人体缺乏维生素A会引起坏血病 | |
| D. | 蛋白质、淀粉、甲烷都是有机高分子化合物 |
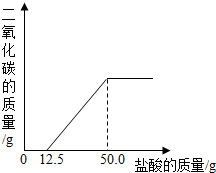 取50.00g某质量分数浓度的NaOH溶液,向其中通入二氧化碳气体后,再向溶液中逐滴滴入18.25%的盐酸,产生CO2气体的质量(假设反应后CO2完全逸出)与所加的盐酸体积之间的关系如图所示.(保留两位小数)
取50.00g某质量分数浓度的NaOH溶液,向其中通入二氧化碳气体后,再向溶液中逐滴滴入18.25%的盐酸,产生CO2气体的质量(假设反应后CO2完全逸出)与所加的盐酸体积之间的关系如图所示.(保留两位小数)