题目内容
18.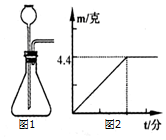 实验室用图1气体发生装置来制取二氧化碳,老师给小李提供了石灰石、无标签的稀盐酸和稀硫酸水溶液各一瓶.
实验室用图1气体发生装置来制取二氧化碳,老师给小李提供了石灰石、无标签的稀盐酸和稀硫酸水溶液各一瓶.(1)要把稀酸选出,可选用下列的D 来检验.
A.硝酸银溶液 B.酚酞试液
C.pH试纸 D.硝酸钡溶液
(2)把石灰石和100克稀酸装进发生器中,用天平称量发生器和里面物质的总质量,发现总质量的减小值m与反应时间t的关系如图2示,最后还有少量石灰石剩余.根据图象,最终生成二氧化碳质量为4.4g.所用稀酸的溶质质量分数是多少?(请写出计算过程.)
分析 实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳,根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
解答 解:(1)要把稀酸选出,可选用下列的硝酸钡溶液来检验,这是因为硝酸钡不能和稀盐酸反应,能和稀硫酸反应生成硫酸钡沉淀和硝酸.
故填:D.
(2)因为碳酸钙和稀硫酸反应生成硫酸钙、水和二氧化碳,生成的硫酸钙微溶于水,会阻止反应进行,因此实验室利用稀盐酸和碳酸钙制取二氧化碳;
最终生成二氧化碳质量为4.4g,
故填:4.4g.
设100g稀盐酸中氯化氢质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
73 44
x 4.4g
$\frac{73}{x}$=$\frac{44}{4.4g}$,
x=7.3g,
所用稀盐酸的溶质质量分数是:$\frac{7.3g}{100g}$×100%=7.3%,
答:所用稀盐酸的溶质质量分数是7.3%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
实验室有不纯的氯酸钾样品12.5 g,把该样品与少量二氧化锰混合加热制取氧气(杂质不参加反应),充分反应后,固体混合物质量变化如下所示:
反应前固体总质量 | 反应后固体总质量 |
13.5g | 8.7 g |
(1)生成氧气的质量为 g;
(2)样品中氯酸钾的质量分数是多少?
9.既能跟稀硫酸反应又能跟熟石灰反应的物质是( )
| A. | 硫酸铜 | B. | 碳酸钠 | C. | 氢氧化钠 | D. | 碳酸钙 |
6.三国时代,诸葛亮领兵南征孟获,遇到了“哑泉”.士兵们饮后致哑、腹痛,甚至死亡.又有一“安乐泉”,与“哑泉”混合后可解“哑泉”之毒.1995年10月,国内某刊报道,经研究,“哑泉”水中溶有CuSO4,而“安乐泉”水质偏碱性.下列有关说法不符合题意的是( )
| A. | “哑泉”之毒是由于水中的Cu2+使人体中的蛋白质变性 | |
| B. | “安乐泉”水质偏碱性,故其泉水中含OH- | |
| C. | “安乐泉”能解“哑泉”之毒的化学反应实质为Cu2++2OH-=Cu(OH)2↓ | |
| D. | “安乐泉”能解“哑泉”之毒的化学反应实质为H++OH-=H2O |
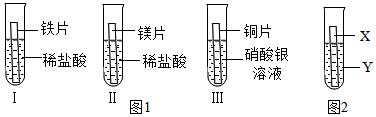
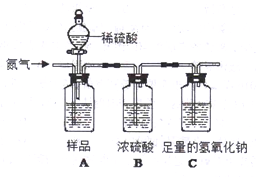 在实验室,小柯看到一瓶长久放置的氢氧化钠固体样品,他想:这瓶氢氧化钠有无变质呢?于是他和小组同学进行了如下探究:
在实验室,小柯看到一瓶长久放置的氢氧化钠固体样品,他想:这瓶氢氧化钠有无变质呢?于是他和小组同学进行了如下探究: