题目内容
10.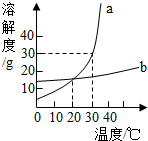 如图为a、b两种固体物质的溶解度曲线,请根据图中信息回答下列问题.
如图为a、b两种固体物质的溶解度曲线,请根据图中信息回答下列问题.(1)a、b两种物质在20℃时溶解度相对较大的是a;
(2)a的溶液中含有少量b时,可用降温结晶(或冷却热饱和溶液) 的方法得到较纯净的a;
(3)30℃时,将30g固体a放入50g水中,得到的溶液是a的饱和溶液(填“饱和”或“不饱和”),该溶液的质量是65 g;
(4)20℃时.将b的不饱和溶液变为饱和溶液的方法是加入b(或恒温蒸发溶剂).
分析 (1)据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(2)据物质的溶解度随温度变化情况可知提纯物质的方法;
(3)据该 温度下物质的溶解度分析解答;
(4)不饱和溶液变为饱和溶液的一般方法是:加入溶质、蒸发溶剂、降温.
解答 解:(1)由溶解度曲线可知:两种物质在20℃时溶解度相对较大的是a;
(2)a的溶解度受温度影响较大,b的溶解度受温度影响较小,所以a溶液中含有少量b时,可用降温结晶或冷却热饱和溶液的方法得到较纯净的a;
(3)30℃时a的溶解度是30g,即100g水中最多溶解30g的a,所以将30g固体a放入50g水中最多溶解15g的a,故所得溶液是a的饱和溶液,该溶液的质量是 65g;
(4)b的溶解度受温度影响不大,所以20℃时将b的不饱和溶液变为饱和溶液的方法是加入溶质或恒温蒸发溶剂;
故答案为:(1)a;(2)降温结晶(或冷却热饱和溶液);(3)饱和;65;(4)加入b(或恒温蒸发溶剂).
点评 明确溶解度概念、溶解度曲线的意义、物质分离的方法、饱和溶液和不饱和溶液的相互转化方法是解答问题的关键.

练习册系列答案
相关题目
3.分类是学习化学的方法之一,下列各组物质按照混合物、氧化物、单质的顺序排列的是( )
| A. | 冰水混合物、干冰、液氢 | B. | 石油、天然气、氧气 | ||
| C. | 生铁、过氧化氢、金刚石 | D. | 硫酸、熟石灰、金属 |
15.下列操作中能发生反应且最终溶液质量增加的是( )
| A. | 将二氧化碳通入澄清石灰水中 | B. | 向饱和的氯化钠溶液中加入硝酸钾 | ||
| C. | 将二氧化硫通入烧碱溶液中 | D. | 将浓硫酸敞口放置于空气中 |
2.在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下.则下列说法中,正确的是
( )
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 4 | 10 | 1 | 25 |
| 反应后质量/g | 未测 | 21 | 10 | 9 |
| A. | X可能是该反应的催化剂 | |
| B. | 若X与Q相对分子质量之比为1:2,则其化学计量数之比也为1:2 | |
| C. | 该反应为分解反应 | |
| D. | 该反应为氧化反应 |
19.表中数据是固体甲在不同温度时的溶解度.现向100g水中不断加入固体甲或改变温度,得到相应的溶液①~⑤:
25℃100g水$→_{37.2g}^{加入甲}$①$→_{4.2g}^{加入甲}$②$→_{至60℃}^{升温}$③$→_{9g}^{加入甲}$④$→_{至50℃}^{降温}$⑤,下列说法正确的是( )
| 资料:甲的溶解度 | |||||
| 温度/℃ | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 |
| A. | ①和②中甲的质量分数相等 | B. | ②和③中都有固体存在 | ||
| C. | ③和⑤的溶液都是饱和溶液 | D. | ④和⑤中没有固体存在 |
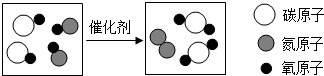 (1)天然气的主要成分是甲烷;地壳中含量最多的金属元素是铝元素.
(1)天然气的主要成分是甲烷;地壳中含量最多的金属元素是铝元素.