题目内容
7.取8克某石灰石样品(杂质不溶于水,与不一盐酸反应),把100克稀盐酸分5次加入样品中,得到的实验数据如表:| 稀盐酸的用量/g | 第1次 加入20 | 第2次 加入20 | 第3次 加入20 | 第4次 加入20 | 第5次 加入20 |
| 剩余固体/g | 6 | 4 | 2 | 1 | m |
②m的数值是1.
③石灰石样品中碳酸钙的质量分数是多少?
④所用稀盐酸的质量分数是多少?
分析 (1)根据每次加入20g的盐酸后,固体质量都减少2g,依据表中的数据进行分析;
(2)根据石灰石样品中的杂质不参与反应,也不溶于水,最后剩余固体的质量就是杂质的质量进行分析;
(3)根据剩余固体和样品的质量计算石灰石样品中碳酸钙的质量分数
(4)根据20g的稀盐酸反应固体的质量计算用稀盐酸的质量分数.
解答 解:(1)通过分析表中的数据可知,每20g盐酸充分反应能反应固体质量是2g,第4加入20g稀盐酸充分反应只反应1g,盐酸有剩余,剩余的固体不与稀盐酸反应;
(2)由上述分析可知,剩余固体的质量是1g,则m的质量为1g;
(3)石灰石样品中CaCO3的质量分数为:$\frac{8g-1g}{8}$×100%=87.5%;
(3)设20g盐酸中溶质的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73
2g x
$\frac{100}{73}=\frac{2g}{x}$ 解得:x=1.46g
所用稀盐酸的质量分数是:$\frac{1.46g}{20g}×100%$=7.3%.
故答案为:(1)4;(2)1;(3)石灰石样品中CaCO3的质量分数为87.5%;(3)盐酸的质量分数为7.3%.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
相关题目
17.氮元素有多种可变化合价.在NH4NO3、N2、NO2、NO、NaNO2这五种物质中N元素表现出的化合价共有( )
| A. | 7种 | B. | 6种 | C. | 5种 | D. | 4种 |
2.市场上出售的牙膏种类繁多,每种牙膏中都添加有细粉末状的摩擦剂,它能配合牙刷一起摩擦牙齿的表面,起到增强清洁牙齿的效果.下表给出了三种牙膏中的摩擦剂.
(1)可选作摩擦剂的物质必须难溶于水(填“易溶于水”或“难溶于水”).
(2)碳酸钙可用石灰石制备,小新设计了两种制备碳酸钙的实验方案.
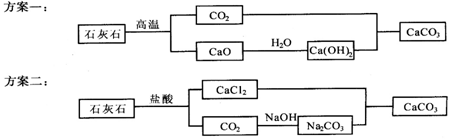
你认为哪一种实验方案更合理,并说明理由方案二,反应在通常情况下进行,生产效率高.
(3)小新为了测定B牙膏中碳酸钙的含量.称取B牙膏100克放入烧杯中,缓慢加入稀盐酸至不再有气泡产生(假设除碳酸钙外,牙膏中的其他物质不与盐酸反应),共用去稀盐酸200克.反应完毕后,称得烧杯内剩余物质的质量为278克.
①在测定中,反应生成的二氧化碳质量为22克.
②请计算牙膏中碳酸钙的质量分数.
| 牙膏 | A | B | C |
| 摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
(2)碳酸钙可用石灰石制备,小新设计了两种制备碳酸钙的实验方案.

你认为哪一种实验方案更合理,并说明理由方案二,反应在通常情况下进行,生产效率高.
(3)小新为了测定B牙膏中碳酸钙的含量.称取B牙膏100克放入烧杯中,缓慢加入稀盐酸至不再有气泡产生(假设除碳酸钙外,牙膏中的其他物质不与盐酸反应),共用去稀盐酸200克.反应完毕后,称得烧杯内剩余物质的质量为278克.
①在测定中,反应生成的二氧化碳质量为22克.
②请计算牙膏中碳酸钙的质量分数.
16.分类是学习化学的方法之一,下列物质是按酸、碱、盐、氧化物的顺序排列的是( )
| A. | 盐酸、熟石灰、食盐、水 | B. | 硫酸、纯碱、硫酸钠、干冰 | ||
| C. | 硝酸、烧碱、碳酸钙、氧气 | D. | 碳酸钙、氨水、硫酸钡、氧化钠 |

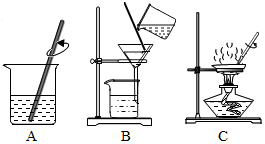
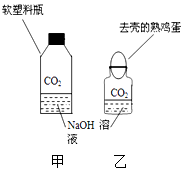 某兴趣小组同学将制得的CO2分别通入澄清石灰水和氢氧化钠溶液中,他们观察到前者变浑浊,后者无明显现象.CO2和NaOH是否发生了化学反应?小明设计了甲、乙两个
某兴趣小组同学将制得的CO2分别通入澄清石灰水和氢氧化钠溶液中,他们观察到前者变浑浊,后者无明显现象.CO2和NaOH是否发生了化学反应?小明设计了甲、乙两个