题目内容
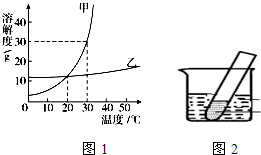 图1是甲、乙两种固体物质的溶解度曲线.回答下列问题:
图1是甲、乙两种固体物质的溶解度曲线.回答下列问题: (1)30℃时,甲物质的溶解度是
(2)当温度为
(3)甲中含有少量的乙,若提纯甲,可采用
(4)将30℃时甲、乙的饱和溶液降温至20℃时,析出晶体的质量为
(5)如图2所示,20℃时,将盛有饱和石灰水的小试管放入盛水的烧杯中,向水中加入某物质后,试管中出现浑浊现象,加入的物质可能是下列中的
A.氢氧化钠固体 B.硝酸铵固体 C.食盐.
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,溶解时的吸热或放热现象
专题:溶液、浊液与溶解度
分析:根据固体的溶解度曲线可以:
(1)查出某种物质在某温度下的溶解度;
(2)比较不同物质在同一温度下的溶解度大小;
(3)判断物质的溶解度随温度变化的变化情况,从而确定通过降温还是蒸发溶剂的方法达到提纯物质的目的;
(4)比较析出晶体质量的大小,必须要确定饱和溶液的质量;
(5)熟石灰的溶解度随温度的升高而减小.
(1)查出某种物质在某温度下的溶解度;
(2)比较不同物质在同一温度下的溶解度大小;
(3)判断物质的溶解度随温度变化的变化情况,从而确定通过降温还是蒸发溶剂的方法达到提纯物质的目的;
(4)比较析出晶体质量的大小,必须要确定饱和溶液的质量;
(5)熟石灰的溶解度随温度的升高而减小.
解答:解:
(1)根据甲物质的溶解度曲线可知,在30℃时,甲物质的溶解度是30g,故答案为:30;
(2)由于在20℃时,两物质的溶解度曲线交于一点,说明两物质的溶解度相等,故答案为:20;
(3)由于甲的溶解度随温度的升高而明显增大,而乙的溶解度受温度的影响很小,因此可以通过降温结晶的方法来提纯混有乙的甲,故答案为:降温结晶;
(4)比较析出晶体质量的大小,必须要确定饱和溶液的质量,将30℃时甲、乙的饱和溶液降温至20℃时,因饱和溶液的质量不确定,故析出晶体的质量无法比较,故选:D;
(5)20℃时,将盛有饱和石灰水的小试管放入盛水的烧杯中,向水中加入某物质后,试管中出现浑浊现象,说明石灰水的溶解度减小了,据熟石灰的溶解度随温度的升高而减小,可确定加入的物质使溶液的温度升高,而氢氧化钠固体溶于水放热,能使溶液温度升高,故选:A.
故答案为:(1)30;(2)20;(3)降温结晶;(4)D;(5)A.
(1)根据甲物质的溶解度曲线可知,在30℃时,甲物质的溶解度是30g,故答案为:30;
(2)由于在20℃时,两物质的溶解度曲线交于一点,说明两物质的溶解度相等,故答案为:20;
(3)由于甲的溶解度随温度的升高而明显增大,而乙的溶解度受温度的影响很小,因此可以通过降温结晶的方法来提纯混有乙的甲,故答案为:降温结晶;
(4)比较析出晶体质量的大小,必须要确定饱和溶液的质量,将30℃时甲、乙的饱和溶液降温至20℃时,因饱和溶液的质量不确定,故析出晶体的质量无法比较,故选:D;
(5)20℃时,将盛有饱和石灰水的小试管放入盛水的烧杯中,向水中加入某物质后,试管中出现浑浊现象,说明石灰水的溶解度减小了,据熟石灰的溶解度随温度的升高而减小,可确定加入的物质使溶液的温度升高,而氢氧化钠固体溶于水放热,能使溶液温度升高,故选:A.
故答案为:(1)30;(2)20;(3)降温结晶;(4)D;(5)A.
点评:本题难度不大,主要考查了固体溶解度曲线的意义,及根据固体的溶解度曲线来解决相关的问题.

练习册系列答案
相关题目
根据下列化学式的规律:HCl、Cl2、( )、HClO3、NaClO4,括号中的化学式为( )
| A、NaCl |
| B、HClO |
| C、HClO4 |
| D、MgCl2 |
下列物质含有氧气的是( )
| A、过氧化氢溶液 | B、高锰酸钾 |
| C、二氧化锰 | D、液态空气 |
下列顺序排列正确的是( )
| A、相对分子质量:二氧化碳>氢气>氮气 |
| B、硫元素的化合价:SO2>Na2SO4>H2S |
| C、核外电子数:钠原子>钠离子 |
| D、地壳中元素含量:Si>Fe>Al |
下列变化中属于物理变化的是( )
| A、水结成冰 | B、白磷自燃 |
| C、食物腐烂 | D、铁生锈 |

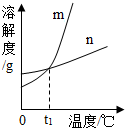 如图是根据NaCl、KNO3两种物质的溶解度绘制的溶解度曲线.
如图是根据NaCl、KNO3两种物质的溶解度绘制的溶解度曲线.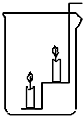 如图:左边向大烧杯中倒入二氧化碳气体,观察到的现象是
如图:左边向大烧杯中倒入二氧化碳气体,观察到的现象是