题目内容
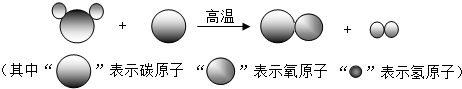
18. 高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.(1)试管尾部放一团湿棉花的目的是提供水蒸气.
(2)探究生成的气体是什么?用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是氢气,写出该反应的化学方程式2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
| 与盐酸反应的产物 | FeCl2+H2O | FeCl3+H2O | FeCl2+FeCl3+H2O |
【猜想与假设】猜想一:剩余固体是FeO或FeO和铁粉;猜想二:剩余固体是Fe3O4或Fe3O4和铁粉.
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引
【实验探究】
| 实验操作 | 实验现象及结论 |
| 取少量黑色固体于试管中,加入足量的稀盐酸. | 若固体全部溶解,没有气泡冒出,剩余固体是Fe3O4. 若固体全部溶解,有气泡冒出,剩余固体是铁粉和四氧化三铁的混合物. |
分析 实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是氢气,因为氢气具有可燃性,氢气和氧气在点燃的条件下生成水,配平即可;实验发现为黑色固体,它不可能是Fe2O3,理由是Fe2O3是红色的;实验发现为黑色固体,铁粉、氧化亚铁、四氧化三铁都是黑色的,因此猜想一:剩余固体是FeO或FeO和铁粉;猜想二:剩余固体是Fe3O4或Fe3O4和铁粉;初步试验:试管中剩余固体为黑色,能全部被磁铁吸引,说明没有氧化亚铁;取少量黑色固体于试管中,加入足量的稀盐酸,若固体全部溶解,没有气泡冒出,剩余固体是四氧化三铁;若固体全部溶解,有气泡冒出,剩余固体是铁粉和四氧化三铁的混合物;因此铁和水蒸气在高温的条件下生成四氧化三铁和氢气,配平即可.
解答 解:(2)本题通过实验资料和实验分析,用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是氢气,因为氢气具有可燃性,氢气和氧气在点燃的条件下生成水,配平即可;故答案为:氢气;2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
(3)【查阅资料】实验发现为黑色固体,它不可能是Fe2O3,理由是Fe2O3是红色的;故答案为:Fe2O3是红色的;
【猜想与假设】故实验发现为黑色固体,铁粉、氧化亚铁、四氧化三铁都是黑色的,因此猜想一:剩余固体是FeO或FeO和铁粉;猜想二:剩余固体是Fe3O4或Fe3O4和铁粉;答案为:FeO或FeO和铁粉;Fe3O4或Fe3O4和铁粉;
【实验探究】取少量黑色固体于试管中,加入足量的稀盐酸,若固体全部溶解,没有气泡冒出,剩余固体是四氧化三铁;若固体全部溶解,有气泡冒出,剩余固体是铁粉和四氧化三铁的混合物;故答案为:稀盐酸;Fe3O4;铁粉和四氧化三铁的混合物;
【实验结论】铁和水蒸气在高温的条件下生成四氧化三铁和氢气,配平即可,故答案为:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;
点评 本考点既考查了实验步骤的设计,又考查了化学方程式的书写,还对实验进行了评价,综合性比较强.实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案| A化学与生活 | B化学与环境 |
| ①生活中常用加热煮沸的方法软化硬水 ②用燃烧的方法区分羊毛和涤纶 ③干冰用于人工降雨 | ①焚烧植物秸秆不会造成空气污染 ②PM2.5是造成雾霾天气的元凶之一 ③含磷洗涤剂的使用会导致水污染 |
| C化学与安全 | D化学与健康 |
| ①点燃可燃性气体前必须验纯 ②在室内放一盆水,可防止煤气中毒 ③夜间发现液化气泄漏开灯寻找泄漏源 | ①人体缺铁会引起贫血 ②用甲醛的水溶液浸泡海产品保鲜 ③食用蔬菜和水果来补充维生素 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 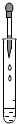 滴加液体 | B. | 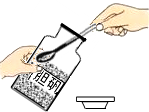 取固体药品 | C. | 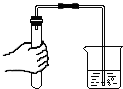 检查气密性 | D. |  熄灭酒精灯 |
| A. | MgCl2溶液 | B. | KNO3溶液 | C. | Na2CO3溶液 | D. | NaOH溶液 |
| A. | 只用酚酞溶液区别盐酸、石灰水和食盐水 | |
| B. | 用熟石灰区别硫酸钾和氯化铵 | |
| C. | 用燃烧的方法区别棉纤维和羊毛纤维 | |
| D. | 用水区别消石灰和苛性钠 |

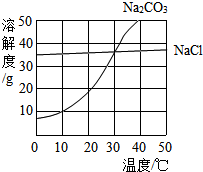 如图为氯化钠、碳酸钠在水中的溶解度曲线,根据图示回答问题.
如图为氯化钠、碳酸钠在水中的溶解度曲线,根据图示回答问题.