题目内容
12. 2010年全国“两会”代表和委员们首次使用环保“石头纸”制作的便笺和文件袋.“石头纸”是一种低碳经济的绿色产品,它的主要成分是一种含钙的盐类化合物.某学习小组对“石头纸”进行如图所示实验,观察到澄清的石灰水变浑浊.请回答下列问题:
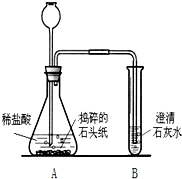
2010年全国“两会”代表和委员们首次使用环保“石头纸”制作的便笺和文件袋.“石头纸”是一种低碳经济的绿色产品,它的主要成分是一种含钙的盐类化合物.某学习小组对“石头纸”进行如图所示实验,观察到澄清的石灰水变浑浊.请回答下列问题:(1)“石头纸”的主要成分是碳酸钙.
(2)装置A、B的反应原理(用化学方程式表示)是:CaCO3+2HCl═CaCl2+H2O+CO2↑,Ca(OH)2+CO2═CaCO3↓+H2O
(3)积极推广使用“石头纸”,可减少二氧化碳气体的排放,有利于缓解引起全球气候异常变化的“温室效应”.
分析 (1)根据题意可知石头纸的主要成分是碳酸钙;
(2)装置A中是盐酸和碳酸钙的反应,而B中是二氧化碳和石灰水的反应,可以直接写出化学方程式;
(3)从减少二氧化碳的排放角度分析.
解答 解:(1)石头纸的主要成分是一种含钙的盐类化合物,能够和盐酸反应生成使澄清石灰水变浑浊的气体,可知石头纸的主要成分为碳酸钙;
(2)根据(1)的判断可以直接写出化学方程式,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,CaCO3+2HCl═CaCl2+H2O+CO2↑ 二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,Ca(OH)2+CO2═CaCO3↓+H2O;
(3)二氧化碳的大量排放会引起温室效应,只要是生活中能够减少碳排放的,积极推广使用“石头纸”,可减少二氧化碳气体的排放.
故答案为:(1)碳酸钙;
(2)CaCO3+2HCl═CaCl2+H2O+CO2↑、Ca(OH)2+CO2═CaCO3↓+H2O;
(3)二氧化碳气体的排放.
点评 熟练掌握碳酸盐的化学性质,记住二氧化碳的检验方法,能正确的写出以下化学方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑,Ca(OH)2+CO2═CaCO3↓+H2O.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.根据要求填空
(1)写出下列物质:
(2)写出下列离子符号:
(1)写出下列物质:
| 名称 | 氢氧化钙 | 硝酸银 | 氯化铝 | 硫酸钡 | 碳酸钙 |
| 化学式 | Ca(OH)2 | AgNO3 | AlCl3 | BaSO4 | CaCO3 |
| 名称 | 亚铁离子 | 碳酸根离子 | 硝酸根离子 | 硫酸根离子 | 硅酸根离子 |
| 离子符号 | Fe2+ | CO32- | NO3- | SO42- | SiO32- |
3.根据下列反应,可判断X、Y、Z三种金属的活动性由强到弱的顺序是( )
Z+Y(NO3)2═Z(NO3)2+Y Z+H2SO4═ZSO4+H2↑
X+Y(NO3)2═X(NO3)2+Y X+H2SO4-不发生反应.
Z+Y(NO3)2═Z(NO3)2+Y Z+H2SO4═ZSO4+H2↑
X+Y(NO3)2═X(NO3)2+Y X+H2SO4-不发生反应.
| A. | Z>X>Y | B. | X>Y>Z | C. | Y>X>Z | D. | Y>Z>X |
4.市政府有关部门提醒大家,冬季燃煤要特别注意室内通风,以免造成人员中毒.这里的有毒气体主要是指( )
| A. | 氮气 | B. | 氧气 | C. | 二氧化碳 | D. | 一氧化碳 |