题目内容
17.按要求完成下列方程式:(1)工业上常用熟石灰和纯碱用来制取烧碱Ca(OH)2+Na2CO3═CaCO3↓+Ca(OH)2.
(2)胃乐新胶囊(主要成分是氢氧化铝)是一种治疗胃酸过多的药物,其反应的化学方程式Al(OH)3+3HCl=AlCl3+3H2O,基本反应类型是复分解反应.
分析 根据反应物、生成物和反应条件及质量守恒定律的两个原则,写出正确的化学方程式.
解答 解:(1)纯碱与氢氧化钙反应生成碳酸钙和氢氧化钙,化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+Ca(OH)2;
(2)胃酸的主要成分是盐酸,盐酸与氢氧化铝反应是中和反应,它属于复分解反应中的一种.胃乐新胶囊中的主要成分与胃酸发生反应的化学方程式
为 Al(OH)3+3HCl=AlCl3+3H2O;
故答案为:(1)Ca(OH)2+Na2CO3═CaCO3↓+Ca(OH)2;(2)Al(OH)3+3HCl=AlCl3+3H2O;复分解反应;
点评 本题难度不大,主要考查了化学方程式的书写,从而加强学生对化学反应的理解.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
12.-些食物的近似pH如下:葡萄3.5--4.5,苹果2.9--3.3,牛奶6.3,--6.6,鸡蛋清7.6--8.0.下列说法错误的是( )
| A. | 胃酸过多的人不应多食苹果 | B. | 葡萄汁能使紫色石蕊试液变蓝 | ||
| C. | 鸡蛋清是碱性食物 | D. | 苹果汁的酸性比葡萄汁强 |
9.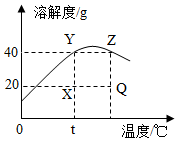 如图是某固态物质的溶解度曲线,图中的4个点分别表示在某条件下,该溶质的溶液所处的一种状况.下列说法正确的是( )
如图是某固态物质的溶解度曲线,图中的4个点分别表示在某条件下,该溶质的溶液所处的一种状况.下列说法正确的是( )
 如图是某固态物质的溶解度曲线,图中的4个点分别表示在某条件下,该溶质的溶液所处的一种状况.下列说法正确的是( )
如图是某固态物质的溶解度曲线,图中的4个点分别表示在某条件下,该溶质的溶液所处的一种状况.下列说法正确的是( )| A. | t℃时该溶质的溶液接近饱和,升温、降温均不能变成饱和溶液 | |
| B. | X、Q点表示溶液的溶质质量分数均为20% | |
| C. | t℃时100g水中最多溶解该物质40g | |
| D. | Y、Z点表示的溶液的溶解度关系是Y<Z |