题目内容
10.制得硫酸亚铁晶体时,利用废铁屑与一定量的稀硫酸反应,并使铁屑过量,请回答下列问题:(1)书写该反应原理的化学方程式Fe+H2SO4═FeSO4+H2↑;
(2)该反应属于基本化学反应类型置换反应;
(3)反应时加入铁屑过量的目的是防止亚铁离子被氧化.
分析 铁与硫酸反应生成了硫酸亚铁和氢气,亚铁离子易被氧化成铁离子,据此分析回答有关的问题.
解答 解:(1)铁与硫酸反应生成了硫酸亚铁和氢气,该反应原理的化学方程式是:Fe+H2SO4═FeSO4+H2↑;
(2)该反应是由一种单质与一种化合物反应生成了另一种单质和另一种化合物,属于置换反应;
(3)由于亚铁离子易被氧化成铁离子,反应时加入铁屑过量的目的是防止亚铁离子被氧化.
故答为:(1)Fe+H2SO4═FeSO4+H2↑;(2)置换反应;(3)防止亚铁离子被氧化.
点评 本题的难度不大,了解铁的性质、反应的特点等知识是解答本题的关键.

练习册系列答案
相关题目
1.日本海啸过后,受灾地区的水源常被严重污染,下列物质中能对被污染的饮用水起杀菌、消毒作用的是( )
| A. | 生石灰 | B. | 明矾 | C. | 木炭 | D. | 漂白粉 |
15.如图操作或装置中没有发生化学变化的是( )
| A. |  O2性质验证 | B. | 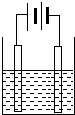 电解水 | ||
| C. |  用玻璃刀裁划玻璃 | D. |  CO2性质验证 |
2.物质X可发生下列所示的两个反应,则X可能是( )
①X+碱→盐+水 ②X+金属氧化物→盐+水.
①X+碱→盐+水 ②X+金属氧化物→盐+水.
| A. | 盐酸 | B. | 一氧化碳 | C. | 氢氧化钠 | D. | 氧化钙 |
20.分析、类比和推理是化学学习中常用的思维方法.下列分析、类比和推理正确的是( )
| A. | 酸雨的pH小于7,所以pH小于7的雨水一定是酸雨 | |
| B. | 酸中都含有氢元素,所以含有氢元素的化合物一定是酸 | |
| C. | 中和反应有盐和水生成,所以有盐和水生成的反应一定是中和反应 | |
| D. | 化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物 |

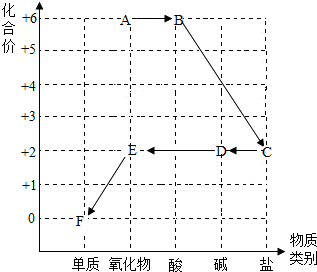 小科以化合价为纵坐标、以物质类别为横坐标绘制了如图,每种物质中都有一种元素的化合价与纵坐标的数值对应,图中字母均表示初中科学中的常见物质,其中“→”表示物质间的转化关系.已知A中氧元素的质量分数为60%,C、D、E、F均含有铜元素.请回答:
小科以化合价为纵坐标、以物质类别为横坐标绘制了如图,每种物质中都有一种元素的化合价与纵坐标的数值对应,图中字母均表示初中科学中的常见物质,其中“→”表示物质间的转化关系.已知A中氧元素的质量分数为60%,C、D、E、F均含有铜元素.请回答: