题目内容
1.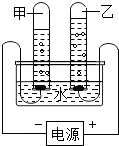 蓉蓉同学按下图做电解水实验,看图回答问题
蓉蓉同学按下图做电解水实验,看图回答问题(1)甲试管中产生的气体为氢气,乙试管中产生的气体为:氧气,检验乙试管中气体的方法为:将带火星的木条伸入试管中,复燃则证明是氧气.
(2)蓉蓉同学做实验时在蒸馏水中加入了适量氢氧化钠溶液,其目的是:增强水的导电性
(3)请写出电解水反应的符号表达式:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑
(4)实验分析:该实验说明水是由氢元素和氧元素组成的.
分析 (1)水通电分解,与电源正极相连的试管产生的为氧气,与负极相连的试管产生氢气,两种气体体积比为1:2;根据氧气的性质分析检验的方法;
(2)根据氢氧化钠在水中能解离出自由移动的离子分析回答;
(3)根据水通电生成氢气和氧气的反应,写出反应的化学方程式;
(4)分析反应后生成物的组成元素,判断水的组成,即该实验能证明的结论.
解答 解:(1)图示的电解水实验中可看到:甲试管内气体约为乙管内气体体积的2倍,则甲管内为氢气,则乙试管产生的气体是氧气,具有助燃性,检验的方法是:将带火星的木条伸入试管中,复燃则证明是氧气.
(2)由于氢氧化钠在水中能解离出自由移动的离子,所以,蓉蓉同学做实验时在蒸馏水中加入了适量氢氧化钠溶液,其目的是:增强水的导电性.
(3)水在通电条件下可分解为氢气和氧气,电解水反应的符号表达式是:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2
(4)氢气由氢元素组成、氧气由氧元素组成,组成氢气和氧气的氢、氧元素均来自水的分解,因此,水由氢、氧元素组成;
故答案为:
(1)氢气,氧气,将带火星的木条伸入试管中,复燃则证明是氧气;
(2)增强水的导电性;
(3)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(4)氢元素,氧元素.
点评 电解水实验的重要现象:与负极相连的试管产生氢气,与电源正极相连的试管产生的为氧气,两种气体体积比为2:1.

练习册系列答案
相关题目
11.在密闭的容器中盛有2g木炭和8g氧气,使其充分反应后,得到气体是( )
| A. | CO2 | B. | CO | C. | CO2和O2 | D. | CO和CO2 |
16.过滤是除去液体中混有的固体物质的方法,下列各组物质可按溶解、过滤、蒸发的顺序,将它们分离的是( )
| A. | 水和酒精 | B. | 食盐和蔗糖 | ||
| C. | 木炭粉和二氧化锰粉末 | D. | 食盐和砂土 |