题目内容
9.下列实验方案中不合理的是( )| A. | 热固性塑料和热塑性塑料-加热,观察外形变化 | |
| B. | 用一氧化碳还原氧化铁留下的黑色物质可用稀盐酸浸泡除去 | |
| C. | 不用其它试剂就能鉴别出硫酸、氯化铁、氢氧化钡、氯化钾和氯化钡 | |
| D. | 为检验敞口放置在空气中的烧碱溶液是否完全变质可先用稀盐酸再用氯化钙溶液 |
分析 A、根据热塑性的物质受热要熔化,而热固性的物质在受热时不易熔化进行分析;
B、根据一氧化碳能把氧化铁还原为黑色的铁粉,铁能与盐酸反应生成可溶的氯化亚铁和氢气分析;
C、首先找到有特殊颜色的物质,先确定出来,然后再用确定出的物质把其它没有确定出的物质确定出来进行分析;
D、根据稀盐酸会和氢氧化钠反应分析.
解答 解:A、热塑性的物质受热要熔化,而热固性的物质在受热时不易熔化,所以可用加热,观察外形变化的方法区别热固性塑料和热塑性塑料,故方案合理;
B、一氧化碳能把氧化铁还原为黑色的铁粉,铁能与盐酸反应生成可溶的氯化亚铁和氢气,固体能除去,故方案合理;
C、首先根据铁离子显黄色鉴别出氯化铁,然后将氯化铁滴入其余四种溶液中,会生成红褐色沉淀的是氢氧化钡,再将氢氧化钡加入剩余的三种溶液中,能够产生白色沉淀的是稀硫酸;再将稀硫酸加入剩下的两种溶液中,能够产生白色沉淀的是氯化钡,无明显现象的是氯化钾,可以鉴别,故方案合理;
D、若先加稀盐酸再加氯化钙溶液,稀盐酸也会把氢氧化钠反应,无法对氢氧化钠的存在进行检验,故方案不合理;
故选项为:D.
点评 本题是对实验设计方案的评价,化学实验方案的设计能够考查学生能力,要求学生能够对其原理透彻理解,学会信息迁移,难度不大.

练习册系列答案
相关题目
19.下列实验操作错误的是( )
| A. | 过滤时玻璃棒斜靠在三层滤纸一边 | |
| B. | 向锥形瓶中添加药品时,先加固体,后加液体 | |
| C. | 在烧杯中溶解氯化钠时用玻璃棒搅拌 | |
| D. | 制取氧气实验中,当导管口开始有气泡冒出时立即收集 |
20.某化学兴趣小组用化学方法测定一种钢样品中铁的含量.同学们称取了5.7g钢样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量也为10.0g)中.在化学反应过程中对烧杯(包括溶液和残余固体)进行了四次称量,记录如表:
(1)反应中产生氢气0.2g克,这种钢样品中铁的含量是多少?(精确到0.1%)
(2)钢的类型分为:含碳质量(C%)0.03%~0.3%为低碳钢;0.3%~0.6%为中碳钢;0.6%~2%为高碳钢.假设残留在烧杯中的黑色固体全部是炭,则这种钢属于高碳钢.
(3)有同学提出:灼烧可使钢中的炭变为CO2挥发掉,灼烧后钢样品质量会减轻.可是他们将一定量的钢样品灼烧后,发现质量反而增加了很多.原因是钢中含碳量少,碳减少的质量远小于铁转化为氧化物增加的质量.
| 反应时间 | t0 | t1 | t2 | t3 |
| 烧杯和药品质量/g | 25.7 | 25.6 | 25.5 | 25.5 |
(2)钢的类型分为:含碳质量(C%)0.03%~0.3%为低碳钢;0.3%~0.6%为中碳钢;0.6%~2%为高碳钢.假设残留在烧杯中的黑色固体全部是炭,则这种钢属于高碳钢.
(3)有同学提出:灼烧可使钢中的炭变为CO2挥发掉,灼烧后钢样品质量会减轻.可是他们将一定量的钢样品灼烧后,发现质量反而增加了很多.原因是钢中含碳量少,碳减少的质量远小于铁转化为氧化物增加的质量.
4.生活中,下列物质的用途与化学性质无关的是( )
| A. | 用氮气保存食品 | B. | 用擦酒精的方法给发热病人降温 | ||
| C. | 用焦炭冶炼金属 | D. | 用小苏打蒸馒头 |
18.化学与生活、环境关系密切,下一有关说法错误的是( )
| A. | 合金不属于合成材料 | |
| B. | 大量排放CO2会导致酸雨 | |
| C. | 煤、石油、天然气是不可再生能源 | |
| D. | 用灼烧法可以区别棉纤维和羊毛纤维 |
19. 某化学兴趣小组同学用实验室中的过氧化钠(Na2O2)粉末进行实验,取少量粉末放入试管中并加入水,观察到有气泡产生,用带火星的木条放在试管口,木条复燃,则该气体是氧气;另取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红.
某化学兴趣小组同学用实验室中的过氧化钠(Na2O2)粉末进行实验,取少量粉末放入试管中并加入水,观察到有气泡产生,用带火星的木条放在试管口,木条复燃,则该气体是氧气;另取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红.
【提出问题】溶液为什么会变红呢?
【查阅资料】过氧化钠与水发生了化学反应,生成碱性物质,碱性物质能使酚酞试液变红.
【猜想假设】甲同学认为生成了碳酸钠; 乙同学认为生成了氢氧化钠.
【实验探究】
(1)小明认为甲同学的猜想无需验证就知道是错误的.他的理由是反应物中不含有碳元素,因此不能生成碳酸钠.
(2)为了证实小明的看法,小组设计了一个证明碳酸钠不存在并验证生成物的实验.
【得出结论】根据实验分析,过氧化钠与水反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑.
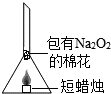
【拓展反思】过氧化钠不仅可以和水发生反应,也可以和二氧化碳反应生成氧气.小红同学又设计了一个如图所示实验(蜡烛火焰与棉花不接触).请回答:
(1)棉花能(填“能”或“不能”)燃烧,这主要是因为蜡烛燃烧生成了能与过氧化钠反应的物质水和二氧化碳,同时反应放热.
(2)结合上述实验事实,请你对运输过氧化钠固体过程中提出一条安全建议:密封保存.
 某化学兴趣小组同学用实验室中的过氧化钠(Na2O2)粉末进行实验,取少量粉末放入试管中并加入水,观察到有气泡产生,用带火星的木条放在试管口,木条复燃,则该气体是氧气;另取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红.
某化学兴趣小组同学用实验室中的过氧化钠(Na2O2)粉末进行实验,取少量粉末放入试管中并加入水,观察到有气泡产生,用带火星的木条放在试管口,木条复燃,则该气体是氧气;另取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红.【提出问题】溶液为什么会变红呢?
【查阅资料】过氧化钠与水发生了化学反应,生成碱性物质,碱性物质能使酚酞试液变红.
【猜想假设】甲同学认为生成了碳酸钠; 乙同学认为生成了氢氧化钠.
【实验探究】
(1)小明认为甲同学的猜想无需验证就知道是错误的.他的理由是反应物中不含有碳元素,因此不能生成碳酸钠.
(2)为了证实小明的看法,小组设计了一个证明碳酸钠不存在并验证生成物的实验.
| 实验操作 | 实验现象 | 实验结论 |
| 取过氧化钠与水反应后的溶液放入试管中,向其中滴加足量稀盐酸. | 无气泡产生 | 不存在碳酸钠 |
| 另取过氧化钠与水反应后的溶液放入试管中,向其中滴加硫酸铜溶液. | 产生蓝色沉淀 | 乙猜想正确 |
【拓展反思】过氧化钠不仅可以和水发生反应,也可以和二氧化碳反应生成氧气.小红同学又设计了一个如图所示实验(蜡烛火焰与棉花不接触).请回答:
(1)棉花能(填“能”或“不能”)燃烧,这主要是因为蜡烛燃烧生成了能与过氧化钠反应的物质水和二氧化碳,同时反应放热.
(2)结合上述实验事实,请你对运输过氧化钠固体过程中提出一条安全建议:密封保存.
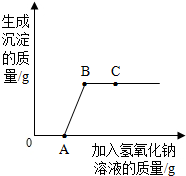 将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,并根据观察到的现象绘制了如图曲线,根据图示回答问题:
将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,并根据观察到的现象绘制了如图曲线,根据图示回答问题: