题目内容
根据质量守恒定律,下列说法正确的是 ( )
A.燃烧的镁带和生成的白色粉末质量相等
B.蜡烛燃烧,固体质量减少,不符合质量守恒定律
C.水分解的质量等于生成的氢气和氧气的质量总和
D.12 g碳在40 g氧气中充分燃烧,一定能生成52 g二氧化碳
【解析】选C。本题主要考查质量守恒定律的内容。参加反应的镁和氧气的质量总和等于生成的白色粉末氧化镁的质量,所以反应的镁的质量应比生成的白色粉末的质量小;任何化学反应都遵循质量守恒定律,蜡烛燃烧生成的二氧化碳和水散失到空气中所以质量减少;质量守恒定律中的“质量”指的是参加化学反应的反应物质量,不是各物质任意质量的简单相加,12 g碳只能和32 g氧气反应生成44 g二氧化碳。

练习册系列答案
相关题目
在一个密闭容器中加入4种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
| 物 质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 2 | 2 | 21 | 5 |
| 反应后质量/g | 10 | 2 | 9 | 待测 |
通过分析,判断下列说法不正确的是 ( )
A.甲是生成物
B.测得反应后丁的质量为4 g
C.乙可能是催化剂
D.该反应是分解反应
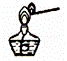
下列实验操作,错误的是( )
|
| A. |
检查装置的气密性 | B. |
读取水的体积 |
|
| C. |
点燃酒精灯 | D. |
倾倒液体 |
 种玉石的主要成分是NaAlSi2O6,下列说法正确的是( )
种玉石的主要成分是NaAlSi2O6,下列说法正确的是( )  10个原子 B.其中硅元素的化合价为-4价
10个原子 B.其中硅元素的化合价为-4价 
 有碳、氢、氧三种元素
有碳、氢、氧三种元素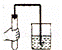
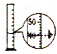
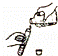
 2C+2D的反应中,14 g A完全反应生成44 g C和18 g D,若A的相对分子质量为28,则B的相对分子质量是 ( )
2C+2D的反应中,14 g A完全反应生成44 g C和18 g D,若A的相对分子质量为28,则B的相对分子质量是 ( )