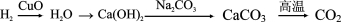题目内容
纳米碳酸钙是一种重要的无机化工产品,下图是某厂生产纳米碳酸钙的工艺流程。

请回答下列问题:
(1)请完成并配平该工艺中生成CaCO3固体的反应方程式:
CaCl2 + ______ + CO2  CaCO3↓ + ______ + H2O
CaCO3↓ + ______ + H2O
(2)若在实验室中进行该实验,操作l的名称是 ,使用到的玻璃仪器有玻璃棒、_____、______,其中玻璃棒的作用是 。
(3)操作2为洗涤、干燥,其中洗涤的目的是除去碳酸钙粗品表面含有的可溶性杂质,其中一定含有的可溶性杂质是 ,检验是否洗涤干净的方法是向最后一次洗涤液中加入 溶液(①Ca(OH)2 、② AgNO3 、③CaCl2,填写序号),如果没有出现沉淀,说明已经洗涤干净。
(4)上述流程中的副产品(NH4Cl)可用作____________肥(填化肥种类)。
(1)2NH3·H2O 、2NH4Cl(不配平不给分)(2)过滤 烧杯 漏斗 引流
(3)NH4Cl(或CaCl2) ② (4)氮(或铵态氮肥)
【解析】
试题分析:(1)根据反应流程可知,该反应的反应物是氯化钙、氨水和二氧化碳,生成物是氯化铵、碳酸钙和水,配平化学方程式的依据是质量守恒定律化学反应前后原子的种类和数目不变,故反应的化学方程式为:CaCl2 + 2NH3·H2O + CO2  CaCO3↓ +2NH4Cl + H2O;
CaCO3↓ +2NH4Cl + H2O;
(2)通过操作1得到了固体和液体,故进行的操作是过滤;过滤时需要的仪器有:玻璃棒、烧杯、铁架台、漏斗,其中玻璃棒起引流的作用;
(3)根据反应的化学方程式可知,可溶性杂质一定含生成的氯化铵,若反应物过量,可能还含有氯化钙;氯化铵和氯化钙中均含有氯离子,氯离子的检验可用硝酸银溶液,若有,会反应生成氯化银白色沉淀;
(4)氯化铵中含有氮元素,属氮肥。
考点:过滤操作,质量守恒定律的应用,物质的检验,化学肥料

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案为了测定某铜、锌合金的组成,称取10g该合金粉末,在粉末中连续6次加入稀硫酸反应,每加一次稀硫酸,记录完全反应后所得剩余固体的质量,实验数据如下:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
剩余固体的质量(g)[ | 8.7 | 7.4 | 6.1 | 4.8 | 3.5 | 3.5 |
(注意:以下各题,只要求填写计算结果,不要求写计算过程)
(1)据表中数据,计算该合金中锌的质量为 ;
(2)计算所加稀硫酸的溶质的质量分数为 (精确到0.1%);
(3)计算恰好完全反应后所得溶液的溶质的质量分数为 (精确到0.1%)。
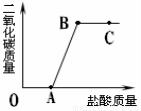
为确认氢氧化钠溶液与稀盐酸反应时,滴加的盐酸是否过量,取少量反应后的溶液于试管中,所用试剂及判断的方法不合理的是
实验方案 | 使用的试剂 | 判断的方法 |
A | 铁粉 | 如果有气泡产生,表明盐酸已经过量 |
B | pH试纸 | 如果pH<7,表明盐酸已经过量 |
C | 硝酸银溶液 | 如果有白色沉淀产生,表明盐酸已经过量 |
D | 紫色石蕊溶液 | 如果溶液变成红色,表明盐酸已经过量 |