题目内容
3. 请根据酸、碱、盐的相关知识,回答下列问题:
请根据酸、碱、盐的相关知识,回答下列问题:(1)农业上常用于改良酸性土壤的一种碱是Ca(OH)2(填化学式).
(2)胃液中含有适量的盐酸.由于胃酸过多而引起的胃痛,可服用含有Mg(OH)2的药物来中和过多的胃酸,发生反应的化学方程式为Mg(OH)2+2HCl=MgCl2+2H2O.
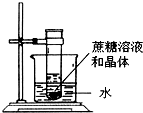
(3)春节喝糖水,一年甜蜜蜜.已知蔗糖的溶解度随温度升高而变大.20℃下,进行如图所示的实验(充分溶解),该蔗糖溶液一定(填“一定”或“不一定”)是饱和溶液.若要让蔗糖固体全部溶解,下列办法可行的是①②⑤(填序号).
①管内加入适量水 ②烧杯内加入适量氢氧化钠固体
③烧杯内加入适量硝酸铵固体 ④恒温蒸发适量水
⑤烧杯中加入适量盐酸和镁条.
分析 (1)酸性土壤一般用碱性物质来中和.选择碱性物质时还要综合考虑这种物质的性质,如是否具有很强的腐蚀性等;
(2)胃液的成分为盐酸,盐酸和氢氧化镁发生中和反应;
(3)根据蔗糖的溶解度随温度的变化分析..
解答 解:(1)熟石灰的主要成分是氢氧化钙,是一种碱性的物质.可用于中和酸性土壤改良土壤结构,其化学式为:Ca(OH)2,
故答案为:Ca(OH)2;
(2)胃液的成分为盐酸,氢氧化镁能与盐酸发生中和反应,生成氯化镁和水,反应为:Mg(OH)2+2HCl=MgCl2+2H2O,中和过多的胃酸,
故答案为:Mg(OH)2+2HCl=MgCl2+2H2O;
(3)由图示可知,有未溶解的蔗糖,该蔗糖溶液一定是饱和溶液.
①试管内加入适量水,能溶解蔗糖,故符合题意;
②烧杯内加入适量氢氧化钠固体,氢氧化钠溶于水放出大量的热,能溶解蔗糖,故符合题意;
③烧杯内加入适量硝酸铵固体,硝酸铵溶于水吸热,会析出的蔗糖,故不符合题意;
④恒温蒸发适量水,会析出蔗糖,故不符合题意;
⑤向烧杯中加入适量盐酸和镁条,盐酸与镁反应放出大量的热,能溶解蔗糖,故符合题意.
故答案为:一定;①②⑤.
点评 本题考查化学与生活联系比较紧密的有关知识,学会利用化学的知识来分析解答问题的方法是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
5. 某学习小组在整理化学试剂时,发现一瓶盛有白色固体的试剂瓶,标签破损(如图).
某学习小组在整理化学试剂时,发现一瓶盛有白色固体的试剂瓶,标签破损(如图).
提出问题:该白色固体的成分是什么?
搜集资料:①经老师回忆,该试剂的酸根离子可能是CO32-、SO32-、SO42-、NO3-中的一种;
②SO2是一种无色有刺激性气味的气体,密度比空气大,易溶于水,能使澄清的石灰水变浑浊,也能使品红溶液褪色,而CO2不能使品红溶液褪色.
猜想假设:该试剂一定不是NaNO3,
可能是Na2SO3,也可能是Na2CO3或Na2SO4.
实验探究:
交流反思:(1)SO2和CO2均属于非金属氧化物,性质相似.请写出下列化学反应方程式:SO2通入澄清石灰水;SO2+Ca(OH)2═CaSO3↓+H2O
(2)亚硫酸钠与盐酸反应能生成SO2,实验室中收集SO2方法是向上排空气法,检验SO2的试剂为品红溶液.
 某学习小组在整理化学试剂时,发现一瓶盛有白色固体的试剂瓶,标签破损(如图).
某学习小组在整理化学试剂时,发现一瓶盛有白色固体的试剂瓶,标签破损(如图).提出问题:该白色固体的成分是什么?
搜集资料:①经老师回忆,该试剂的酸根离子可能是CO32-、SO32-、SO42-、NO3-中的一种;
②SO2是一种无色有刺激性气味的气体,密度比空气大,易溶于水,能使澄清的石灰水变浑浊,也能使品红溶液褪色,而CO2不能使品红溶液褪色.
猜想假设:该试剂一定不是NaNO3,
可能是Na2SO3,也可能是Na2CO3或Na2SO4.
实验探究:
| 实验操作 | 现象 | 结论 |
| (1)取少量白色固体加入适量盐酸 | 产生气泡 | 该白色固体不可能是Na2SO4 |
| (2)产生的气体通入澄清石灰水 | 石灰水变浑浊 | |
| (3)产生的气体通入品红溶液 | 溶液褪色 | 该白色固体是Na2SO3 |
(2)亚硫酸钠与盐酸反应能生成SO2,实验室中收集SO2方法是向上排空气法,检验SO2的试剂为品红溶液.
6.如表是小华对自己吸入的气体和呼出的气体进行探究的结果(体积分数)
(1)请你判断:X是氮气,Y是氧气.
(2)请你回答:因参与新陈代谢而被人体消耗的是氧气.
(3)请你证明:呼出气体中含有水蒸气.你的实验方法是对着干冷的玻璃片上呼气.
(4)请你分析:X气体在呼吸过程中没有参与化学反应,但呼出气体中体积分数却减少了,原因是氮气的体积含量减少主要是由于二氧化碳和水蒸气等气体的含量增加引起的.
| 气体 | X | Y | 二氧化碳 | 水蒸气 |
| 吸入气体 | 78.25% | 21.05% | 0.04% | 0.66% |
| 呼出气体 | 74.88% | 15.26% | 3.68% | 6.18% |
(2)请你回答:因参与新陈代谢而被人体消耗的是氧气.
(3)请你证明:呼出气体中含有水蒸气.你的实验方法是对着干冷的玻璃片上呼气.
(4)请你分析:X气体在呼吸过程中没有参与化学反应,但呼出气体中体积分数却减少了,原因是氮气的体积含量减少主要是由于二氧化碳和水蒸气等气体的含量增加引起的.
3.铝锅中长期盛放食醋,以下说法正确的是( )
| A. | 铝是有毒元素,对人体健康有害;长期存放食醋的铝锅也会受到食醋的腐蚀而显受损,易折断 | |
| B. | 铝是非金属材料,在酸性溶液中会发生化学变化 | |
| C. | 铝跟食醋反应生成了剧毒物质,会导致食醋不能食用 | |
| D. | 铝会溶解在食醋中,更有利于人体健康、帮助消化 |
13.学习了溶液的概念后,老师的提问及同学的回答如图1所示:

(1)以上三位同学中描述溶液特征错误的是甲、乙同学.
从200mL20%硝酸钾溶液取出20mL后,剩余溶液为18%,这个答案是正确还是错误的:错误的
老师接着问:“你们还想知道什么?”
甲同学回答:“不溶于水的物质能溶于其他溶剂吗?”
乙同学回答:“影响物质在水中溶解能力的因素有哪些?”
(2)如果让你用实验回答甲同学的问题,老师取溶质油脂,你应该选择的溶剂是汽油.
(3)针对乙同学的问题,老师引导同学们进行了一系列探究,包括绘制A、B、C三种固体物质的溶解度曲线,如表列出了从探究实验中获取的部分数据,乙同学根据表中的数据绘制了一条溶解曲线,它是A物质的溶解度曲线.
根据从这个实验探究中可以说出影响固体物质溶解度大小的有固体颗粒大小、搅拌或温度等.

(1)以上三位同学中描述溶液特征错误的是甲、乙同学.
从200mL20%硝酸钾溶液取出20mL后,剩余溶液为18%,这个答案是正确还是错误的:错误的
老师接着问:“你们还想知道什么?”
甲同学回答:“不溶于水的物质能溶于其他溶剂吗?”
乙同学回答:“影响物质在水中溶解能力的因素有哪些?”
(2)如果让你用实验回答甲同学的问题,老师取溶质油脂,你应该选择的溶剂是汽油.
(3)针对乙同学的问题,老师引导同学们进行了一系列探究,包括绘制A、B、C三种固体物质的溶解度曲线,如表列出了从探究实验中获取的部分数据,乙同学根据表中的数据绘制了一条溶解曲线,它是A物质的溶解度曲线.
| 温度 | 溶解度(g) | ||
| A | B | C | |
| 20 | 16 | 20 | 40 |
| 40 | 30 | 25 | 30 |
| 60 | 53.5 | 30 | 20 |
 t2℃时,向盛有10mL水的A、B两试管中分别加入等质量的甲、乙两种可溶性固体,使其充分溶解后,观察到如图一所示的现象,请回答:
t2℃时,向盛有10mL水的A、B两试管中分别加入等质量的甲、乙两种可溶性固体,使其充分溶解后,观察到如图一所示的现象,请回答: 控制变量法是常用的化学学习方法.下面是探究燃烧条件的实验,请你根据图示信息和资料信息回答有关问题.
控制变量法是常用的化学学习方法.下面是探究燃烧条件的实验,请你根据图示信息和资料信息回答有关问题.
 .
.