题目内容
8.(1)写出下列物质的化学式:①小苏打:NaHCO3;②硫酸铵:(NH4)2SO4.
(2)写出下列反应的化学方程式:
①将铜放在硝酸银溶液中:Cu+2AgNO3=2Ag+Cu(NO3)2.
②碳酸钾溶液和氢氧化钙溶液的反应:K2CO3+Ca(OH)2=CaCO3↓+2KOH.
分析 (1)根据常见元素的化合价来书写化合物的化学式;
(2)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答 解:(1)小苏打是碳酸氢钠的俗称,其中钠元素显+1价,氢元素显+1价,碳酸根显-2价,故填:NaHCO3;
硫酸铵中铵根显+1价,硫酸根显-2价,其化学式为(NH4)2SO4.
(2)①铜与硝酸银溶液反应生成银和硝酸铜,故填:Cu+2AgNO3=2Ag+Cu(NO3)2;
②碳酸钾与氢氧化钙反应生成碳酸钡白色沉淀和氢氧化钾,故填:K2CO3+Ca(OH)2=CaCO3↓+2KOH.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
9.物质的性质与所对应的用途没有直接关系的是( )
| A. | 稀有气体通电能发出有色光--可作保护气 | |
| B. | 甲烷具有可燃性--可作燃料 | |
| C. | 石墨能导电--可作电极 | |
| D. | 干冰升华吸热--可用于人工降雨 |
19.下列对原子的认识正确的是( )
| A. | 原子是构成物质的最小微粒 | |
| B. | 原子是构成一切物质的基本微粒 | |
| C. | 原子是化学变化中的最小微粒 | |
| D. | 原子是可分割成更小微粒的空心小球 |
3.下列关于实验操作或实验现象的描述正确的是( )
| A. | 测定未知溶液的酸碱度时,可以将pH试纸直接伸到待测溶液中 | |
| B. | 将氢氧化钠固体放在托盘天平的左盘滤纸上称量 | |
| C. | 如果皮肤上不慎沾上浓硫酸,应立即用大量的NaOH稀溶液冲洗 | |
| D. | 油脂易使人发胖,故我们要少食用含油脂的食物 |
13.如图所示操作中,正确的是( )
| A. |  倾倒液体 倾倒液体 | B. |  加热液体 加热液体 | C. |  蒸发食盐水 蒸发食盐水 | D. |  稀释浓硫酸 稀释浓硫酸 |
20.下列关于物质分类的说法正确的是( )
| A. | 导电的物质都是金属 | B. | 有一定熔点的固体都是晶体 | ||
| C. | 橡胶、塑料都是合成材料 | D. | 含氧元素的化合物都是氧化物 |
17.下列实验操作与预期实验目的或所得实验结论一致的是( )
| 选项 | 实验操作及现象 | 实验目的或结论 |
| A | 向1,2两试管中分别加入等浓度H2O2溶液10mL、1mL,再向H2O2溶液中分别滴入等浓度等体积CuSO4、FeCl3溶液;试管2中产生气体较快 | 证明FeCl3溶液的催化效率 更高 |
| B | 将洁净的铁钉在饱和食盐水中浸泡一段时间;铁钉上有气泡产生 | 证明铁发生析氢腐蚀 |
| C | 测定物质的量浓度相同的盐酸和醋酸溶液的pH;盐酸pH小于醋酸pH | 证明盐酸酸性比醋酸强 |
| D | 硅酸钠溶液中滴入酚酞,溶液变红,再滴加稀盐酸,溶液红色变浅直至消失 | 证明非金属性:Cl>Si |
| A. | A | B. | B | C. | C | D. | D |
18.溶液在生产、生活中起着十分重要的作用.下列有关溶液的说法中,正确的是( )
| A. | 不饱和溶液转化为饱和溶液,其溶质的质量分数一定增大 | |
| B. | 饱和溶液析出晶体后,溶质的质量分数一定减小 | |
| C. | 只要温度不变,某饱和溶液中固体溶质的溶解度一定不变 | |
| D. | 降温时,饱和溶液一定会析出晶体 |
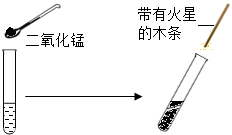 小华学习了双氧水(过氧化氢俗称双氧水)制氧气的实验后,想起自己家里也有一瓶消毒用双氧水,由于标签已部分受损无法判断是否变质,他将该瓶溶液带到学校,进行了如图所示的探究.试回答:
小华学习了双氧水(过氧化氢俗称双氧水)制氧气的实验后,想起自己家里也有一瓶消毒用双氧水,由于标签已部分受损无法判断是否变质,他将该瓶溶液带到学校,进行了如图所示的探究.试回答: