题目内容
11.存放下列物质时,必须密闭的是( )①浓H2SO4 ②Ca(OH)2固体 ③盐酸 ④硝酸钾.
| A. | ① | B. | ①② | C. | ①②③ | D. | ①②③④ |
分析 容易变质或易吸水和易挥发的物质需要密封保存,根据各物质的性质进行判断即可.
解答 解:①浓硫酸具有吸水性,需要密封保存;②氢氧化钙会与空气中的二氧化碳反应生成碳酸钙,需要密封保存;③盐酸易挥发,需要密封保存;④硝酸钾在空气中无任何变化,不需要密封保存.
故选C.
点评 此题是常见物质性质的考查,解题的关键是能知道四种物质中哪些能在空气中会有所变化,属基础性知识考查题.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
1.鉴别下列各组物质,所用试剂不正确的是( )
| 选项 | 待鉴别的物质 | 鉴别试剂 |
| A | 铜和黄铜 | 稀盐酸 |
| B | 海水和蒸馏水 | 硝酸银溶液 |
| C | 澄清的石灰水和氢氧化钠溶液 | 二氧化碳 |
| D | 碳酸钠溶液和氢氧化钠溶液 | 无色酚酞试液 |
| A. | A | B. | B | C. | C | D. | D |
2.以下四组离子,有一组能大量共存且能形成无色透明溶液,它应该是( )
| A. | Fe3+ SO42- H+ Cl- | B. | Mg2+ Cl- OH- Na+ | ||
| C. | H+ Na+ K+ NO3- | D. | H+ Ba2+ NO3- SO42- |
19.下列物质可以由金属与酸反应制得的是( )
| A. | 氯化银 | B. | 硫酸锌 | C. | 氯化铁 | D. | 硫酸铜 |
6.要验证铜、银、铁三种金属活动性顺序时,不能选用哪组物质进行实验( )
| A. | 银、铜、硝酸亚铁 | B. | 银、铜、铁、硫酸铜 | ||
| C. | 银、铁、硫酸铜 | D. | 铜、硝酸亚铁、硝酸银 |
3.高铁酸钠(Na2FeO4)是一种新型高效的水处理剂.下列有关高铁酸钠的说法正确的是( )
| A. | 其相对原子质量为165 | |
| B. | 其中钠、铁、氧三种元素质量比是2:1:4 | |
| C. | 其一个分子中含有7个原子 | |
| D. | 其中铁元素的质量分数为27.71% |
20.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开始探究活动.以下是教学片断,请你参与学习并帮助填写空格(包括表中空格).
【查阅资料】Na2SO4溶液呈中性
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O.
Ⅰ.定性探究
【提出问题】反应后溶液中溶质是什么呢?
【猜想】针对疑问大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的,你认为不合理的猜想是哪种并说出理由猜想四H2SO4和NaOH在溶液中不能共存.
【继续试验】(1)丙组同学取烧杯中的少量溶液于试管中,滴加几滴酚酞溶液,无明显变化,溶液中一定没有NaOH或氢氧化钠.
(2)为了验证其余猜想,各组同学取烧杯中的溶液,丙选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,分别进行如下三组探究实验.
【得出结论】通过探究,全班同学一直确定猜想二是正确的.
【评价反思、老师对同学能用多种方法进行探究,并且得出正确结论给予肯定,同时也指出上述三个实验探究中也有一个是不合理的,这个方案是③(选填①、②、③),你还可以选择锌粒(填药品名称)进行实验,也能得出同样的结论.
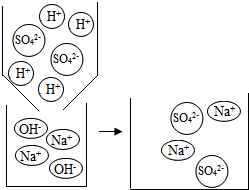
【剖析本质】实验后,老师又带领大家从微观的角度来理解此反应的实质,请你和同学们一起在反应后的方框中补画未画全的微粒.
Ⅰ.定量探究
取上述【演示实验】反应后烧杯中的溶液100g,设计如下实验:
试计算上述【演示实验】反应后溶液中Na2SO4的质量分数是多少?(列出计算过程)
【查阅资料】Na2SO4溶液呈中性
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O.
Ⅰ.定性探究
【提出问题】反应后溶液中溶质是什么呢?
【猜想】针对疑问大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的,你认为不合理的猜想是哪种并说出理由猜想四H2SO4和NaOH在溶液中不能共存.
【继续试验】(1)丙组同学取烧杯中的少量溶液于试管中,滴加几滴酚酞溶液,无明显变化,溶液中一定没有NaOH或氢氧化钠.
(2)为了验证其余猜想,各组同学取烧杯中的溶液,丙选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,分别进行如下三组探究实验.
| 实验方案 | ①测溶液pH | ②滴加Na2CO3溶液 | ③滴加BaCl2溶液 |
| 实验现象 | 试纸变色,与标准比色卡比照,得pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【评价反思、老师对同学能用多种方法进行探究,并且得出正确结论给予肯定,同时也指出上述三个实验探究中也有一个是不合理的,这个方案是③(选填①、②、③),你还可以选择锌粒(填药品名称)进行实验,也能得出同样的结论.
【剖析本质】实验后,老师又带领大家从微观的角度来理解此反应的实质,请你和同学们一起在反应后的方框中补画未画全的微粒.

Ⅰ.定量探究
取上述【演示实验】反应后烧杯中的溶液100g,设计如下实验:

试计算上述【演示实验】反应后溶液中Na2SO4的质量分数是多少?(列出计算过程)