题目内容
2.用如下装置完成对实验室制取二氧化碳实验后剩余固体中钙元素的回收.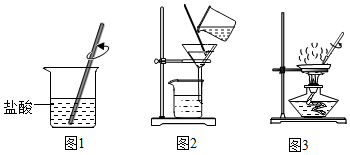
(1)图1装置中操作的目的是把没有反应的碳酸钙转化为氯化钙;
(2)经过上图三步操作,最终钙元素是以氯化钙(填一种物质名称)的形式得以回收.
分析 (1)根据不反应的碳酸钙能与盐酸反应生成氯化钙考虑;(2)根据溶解、过滤、蒸发得到的是氯化钙.
解答 解:(1)不反应的碳酸钙能与盐酸反应生成氯化钙,所以图1装置中操作的目的是把没有反应的碳酸钙转化为氯化钙;
(2)溶解、过滤把不溶性杂质除掉、蒸发得到的是氯化钙.
故答案为:(1)把没有反应的碳酸钙转化为氯化钙;(2)氯化钙.
点评 解答本题关键是知道溶解、过滤、蒸发各步的作用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.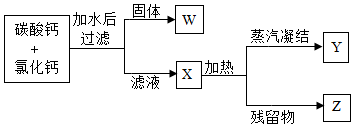 碳酸钙和氯化钙两种固体粉末混合,图为此混合粉末分离的实验步骤,则图中W、X、Y、Z主要各为何种物质?( )
碳酸钙和氯化钙两种固体粉末混合,图为此混合粉末分离的实验步骤,则图中W、X、Y、Z主要各为何种物质?( )
 碳酸钙和氯化钙两种固体粉末混合,图为此混合粉末分离的实验步骤,则图中W、X、Y、Z主要各为何种物质?( )
碳酸钙和氯化钙两种固体粉末混合,图为此混合粉末分离的实验步骤,则图中W、X、Y、Z主要各为何种物质?( )| A. | W为碳酸钙、Y为水、Z为氯化钙 | |
| B. | W为碳酸钙、Y为氯化钙、Z为水 | |
| C. | X为氯化钙水溶液、Y为碳酸钙、Z为水 | |
| D. | X为氯化钙水溶液、Y为水、Z为碳酸钙 |
10.屠呦呦带领科研团队研发的新型抗拒疾药--青蒿素和双氢青蒿素,在全球抗击疟疾进程中,拯救了上百万人的生命.因此获得2015年诺贝尔生理学或医学奖.青蒿素化学式为Cl5H22O5,下列说法不正确的是( )
| A. | 靑蒿素是由15个碳原子,22个氢原子和5个氧原子构成 | |
| B. | 青蒿素中C、H、O三种元素的质量比为90:11:40 | |
| C. | 青蒿素所含元素中碳元素的质量分数最高 | |
| D. | 利用化学提取和合成药物,以抑制细菌和病毒,保障人体健康 |
7.生活中的下列变化.与其他三种变化不同的是( )
| A. | 农家肥的腐熟 | B. | 燃放烟花 | C. | 苹果榨汁 | D. | 酿造米酒 |
14.下列整理的有关化学知识不完全正确的一组是( )
| A.实验安全 | B.化学与环境 |
| 不能凑到容器口闻药品的气味 皮肤上沾到浓硫酸时.先用大量水冲洗后再涂小苏打溶液 点燃甲烷之前先验纯 | 空气中二氧化碳剧增时会形成酸雨 减少化石燃料的使用,开发新能源 科学合理地使用化肥和农药 |
| C.化学之最 | D.物质的性质及川途 |
| 熔点最低的金属是汞 年产量最高的金属是铁 天然存在的最硬物质是金刚石 | 氧气有助燃性---作燃料的助燃剂 干冰升华吸热---人工降雨 熟石灰呈碱性---改良酸性土壤 |
| A. | A | B. | B | C. | C | D. | D |
11. 海洋是地球上最大的储水库,蕴含着丰富的化学资源.海水晒盐能够得到粗盐和卤水.
海洋是地球上最大的储水库,蕴含着丰富的化学资源.海水晒盐能够得到粗盐和卤水.
①卤水中含有MgCl2、KCl和MgSO4等物质,如图是三种物质的溶解度曲线.t2℃时,三种物质的饱和溶液中,溶质质量分数最小的是氯化钾.
②将t2℃时三种物质的饱和溶液加热到t3℃以上时,仍然为饱和溶液的是硫酸镁.
③将饱和氯化镁溶液由t3℃冷却至t1℃,下列四种叙述中,正确的是Ⅱ、Ⅳ(填序号).
④在t3℃时,60克KCl的饱和溶液与60克MgCl2的饱和溶液中,溶质MgCl2与KCl的质量比为3:1,则t3℃时MgCl2的溶解度为100g.
 海洋是地球上最大的储水库,蕴含着丰富的化学资源.海水晒盐能够得到粗盐和卤水.
海洋是地球上最大的储水库,蕴含着丰富的化学资源.海水晒盐能够得到粗盐和卤水.①卤水中含有MgCl2、KCl和MgSO4等物质,如图是三种物质的溶解度曲线.t2℃时,三种物质的饱和溶液中,溶质质量分数最小的是氯化钾.
②将t2℃时三种物质的饱和溶液加热到t3℃以上时,仍然为饱和溶液的是硫酸镁.
③将饱和氯化镁溶液由t3℃冷却至t1℃,下列四种叙述中,正确的是Ⅱ、Ⅳ(填序号).
| Ⅰ.溶液的质量不变 | Ⅱ.氯化镁的溶解度变小 |
| Ⅲ.溶液中溶质质量分数不变 | Ⅳ.溶液中溶质质量分数变小 |