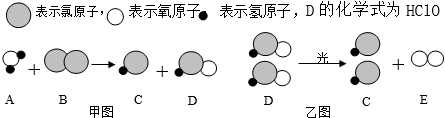
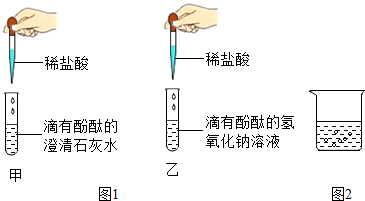
题目内容
14.下列各组物质能共存于同一溶液的是( )| A. | CuCl2、KNO3、NaOH | B. | HCl、K2SO4、Na2CO3 | ||
| C. | NaNO3、KCl、(NH4)2SO4 | D. | HCl、KNO3、NaOH |
分析 根据复分解反应发生的条件可知,若物质之间相互交换成分不能生成水、气体、沉淀,则能够在溶液中大量共存,据此进行分析判断即可.
解答 解:A、NaOH和CuCl2在溶液中相互交换成分生成氢氧化铜沉淀和氯化钠,不能大量共存,故选项错误.
B、Na2CO3和HCl在溶液中能相互交换成分生成氯化钠、水和二氧化碳,不能大量共存,故选项错误.
C、三种物质在溶液中相互交换成分不能生成沉淀、气体、水,能在溶液中大量共存,故选项正确.
D、HCl和NaOH在溶液中能相互交换成分生成氯化钠和水,不能大量共存,故选项错误.
故选C.
点评 本题考查物质的共存问题,判断物质在溶液中能否共存,主要看溶液中的各物质之间能否发生反应生成沉淀、气体、水.

练习册系列答案
相关题目
9.下列物质溶解在水里,当温度升高时,溶解度降低的是( )
| A. | NaCl | B. | Na2CO3 | C. | O2 | D. | KNO3 |
19.锌及其氧化物(ZnO,白色,难溶于水,溶于强酸)具有广泛的应用.
(一)锌的广泛应用
(1)锌被称之为“生命元素”.儿童、青少年如果缺锌严重,将会导致“侏儒 症”和智力发育不良.经常吃贝壳类海产品、红色肉类等含锌的食物有利补“锌”.这里的“锌”是指B.
A.单质 B.元素 C.原子 D.分子
(2)实验室用锌与稀硫酸制取氢气,反应的化学方程式为Zn+H2SO4═ZnSO4+H2↑.
(3)锌与铜熔合可形成“黄铜”,它属于A(选填序号).
A.金属材料 B.无机非金属材料 C.合成材料 D.复合材料
(二)活性ZnO制取的探究
[实验方案]工业上用粗氧化锌(含少量FeO)制取活性氧化锌,其流程如图1:

[查阅资料]一些阳离子以氢氧化物形式开始沉淀、完全沉淀时溶液的pH如表.
[问题探究]
(4)“溶解”前将粗氧化锌粉碎成细颗粒,目的是增大接触面积,使其充分反应.
(5)“溶解”后得到的酸性溶液中含有ZnSO4、H2SO4、FeSO4.除铁池中加入适量H2O2,使Fe2+转化为Fe3+;为使溶液中Fe3+全部转化为Fe(OH)3,而Zn2+不形成Zn(OH)2,则应加入氨水控制溶液的pH的范围为3.2~6.2.
(6)“沉淀池”中的沉淀经过滤、洗涤等操作得纯净固体M,其组成为:aZnCO3•bZn(OH)2•cH2O.
确认固体M已经洗涤干净的操作是:取最后一次洗涤液,最好选择下列C,
向其中滴入无现象,则已经洗干净.
A.紫色石蕊试液 B.少量稀盐酸 C.氯化钡溶液或硝酸钡溶液
[组成测定]固体B的组成会影响制得的ZnO的活性.为确定aZnCO3•bZn(OH)2•cH2O的组成,进行如下实验(假设每步反应、吸收均完全):
[查阅资料]aZnCO3•bZn(OH)2•cH2O受热分解生成ZnO、H2O、CO2三种产物.
(7)写出装置B中发生反应的化学方程式aZnCO3•bZn(OH)2•cH2O$\frac{\underline{\;\;△\;\;}}{\;}$(a+b)ZnO+(b+c) H2O+aCO2↑.现称取35.9g aZnCO3•bZn(OH)2•cH2O在B装置中进行完全煅烧,测得装置C和D的质量分别增重7.2g和4.4g.
[实验分析及数据处理]
(8)装置A的作用是吸收空气中的水和二氧化碳.
(9)根据上述数据,则生成ZnO的质量为24.3g;a:b:c=1:2:2.
(10)若没有E装置,则测得的a值偏大(填“偏大”、“偏小”或“不变”).
(一)锌的广泛应用
(1)锌被称之为“生命元素”.儿童、青少年如果缺锌严重,将会导致“侏儒 症”和智力发育不良.经常吃贝壳类海产品、红色肉类等含锌的食物有利补“锌”.这里的“锌”是指B.
A.单质 B.元素 C.原子 D.分子
(2)实验室用锌与稀硫酸制取氢气,反应的化学方程式为Zn+H2SO4═ZnSO4+H2↑.
(3)锌与铜熔合可形成“黄铜”,它属于A(选填序号).
A.金属材料 B.无机非金属材料 C.合成材料 D.复合材料
(二)活性ZnO制取的探究
[实验方案]工业上用粗氧化锌(含少量FeO)制取活性氧化锌,其流程如图1:

[查阅资料]一些阳离子以氢氧化物形式开始沉淀、完全沉淀时溶液的pH如表.
| 沉淀物 | Fe(OH)3 | Zn(OH)2 | Fe(OH)2 |
| 开始沉淀pH | 1.5 | 6.2 | 6.3 |
| 完全沉淀pH | 3.2 | 8.0 | 9.7 |
(4)“溶解”前将粗氧化锌粉碎成细颗粒,目的是增大接触面积,使其充分反应.
(5)“溶解”后得到的酸性溶液中含有ZnSO4、H2SO4、FeSO4.除铁池中加入适量H2O2,使Fe2+转化为Fe3+;为使溶液中Fe3+全部转化为Fe(OH)3,而Zn2+不形成Zn(OH)2,则应加入氨水控制溶液的pH的范围为3.2~6.2.
(6)“沉淀池”中的沉淀经过滤、洗涤等操作得纯净固体M,其组成为:aZnCO3•bZn(OH)2•cH2O.
确认固体M已经洗涤干净的操作是:取最后一次洗涤液,最好选择下列C,
向其中滴入无现象,则已经洗干净.
A.紫色石蕊试液 B.少量稀盐酸 C.氯化钡溶液或硝酸钡溶液
[组成测定]固体B的组成会影响制得的ZnO的活性.为确定aZnCO3•bZn(OH)2•cH2O的组成,进行如下实验(假设每步反应、吸收均完全):
[查阅资料]aZnCO3•bZn(OH)2•cH2O受热分解生成ZnO、H2O、CO2三种产物.
(7)写出装置B中发生反应的化学方程式aZnCO3•bZn(OH)2•cH2O$\frac{\underline{\;\;△\;\;}}{\;}$(a+b)ZnO+(b+c) H2O+aCO2↑.现称取35.9g aZnCO3•bZn(OH)2•cH2O在B装置中进行完全煅烧,测得装置C和D的质量分别增重7.2g和4.4g.
[实验分析及数据处理]
(8)装置A的作用是吸收空气中的水和二氧化碳.
(9)根据上述数据,则生成ZnO的质量为24.3g;a:b:c=1:2:2.
(10)若没有E装置,则测得的a值偏大(填“偏大”、“偏小”或“不变”).
3.酸、碱和盐的溶解性表(室温)是化学学习的重要工具.下表列出了部分酸、碱、盐在室温时的溶解性,请根据此表信息回答下列问题.
(1)写出硫酸钠的化学式Na2SO4;
(2)只用水就能区分碳酸钡和氯化钙的原因是它们的溶解性不同;
(3)在实验室里浓硝酸要密封保存,原因是浓硝酸有挥发性;
(4)判断硝酸铜溶液与氢氧化钠溶液能否反应,若能反应,写出化学方程式及反应现象,若不能,说明理由2NaOH+Cu(NO3)2=Cu(OH)2↓+2NaNO3;生成蓝色沉淀.
| OH- | Cl- | CO32- | SO42- | NO3- | |
| H+ | 溶、挥 | 溶、挥 | 溶 | 溶、挥 | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Cu2+ | 不 | 溶 | - | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 不 | 不 | 溶 |
| Ca2+ | 微 | 溶 | 不 | 微 | 溶 |
(2)只用水就能区分碳酸钡和氯化钙的原因是它们的溶解性不同;
(3)在实验室里浓硝酸要密封保存,原因是浓硝酸有挥发性;
(4)判断硝酸铜溶液与氢氧化钠溶液能否反应,若能反应,写出化学方程式及反应现象,若不能,说明理由2NaOH+Cu(NO3)2=Cu(OH)2↓+2NaNO3;生成蓝色沉淀.
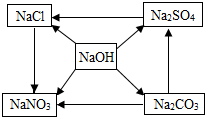 有五种化合物,它们两两之间发生的某些转化关系如图箭头所示.请回答:
有五种化合物,它们两两之间发生的某些转化关系如图箭头所示.请回答: