题目内容
3.A~G是初中化学常见的物质,它们存在如图所示的关系(“一”表示两物质间能反应,“→”表示一种物质转化成另一种物质).部分生成物和反应条件已略,A、B、C三种物质中都含有碳元素,A为黑色固体,:E为常用的建筑材料,F为红色固体.回答下列问题: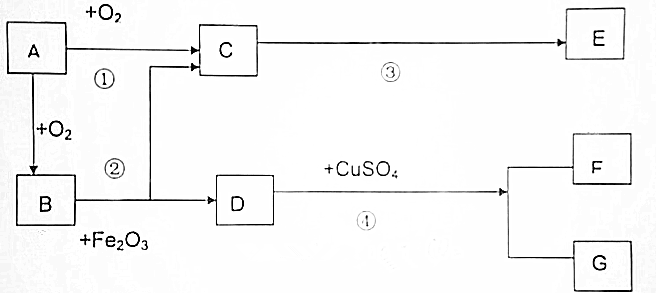
(1)写出F的化学式Cu,物质类别是:金属
(2)写出反应①的化学方程式:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,反应类型为:化合反应
(3)写出反应④的化学方程式为Fe+CuSO4═FeSO4+Cu,该反应的实验现象是:在铁的表面有红色物质生成,溶液由蓝色逐渐变为浅绿色
(4)B通入Fe2O3前的实验操作是:检查装置的气密性
(5)B使人容易中毒的原因是:能与人体中的血红蛋白结合,使人体缺氧.
分析 根据“A、B、C三种物质中都含有碳元素,A为黑色固体”,而A与氧气反应生成C;C可反应生成白色沉淀E;而A与氧气反应生成B;而B与氧化铁反应生成C和D,说明B具有还原性;而D与硫酸铜溶液反应生成红色固体F和G.则推测个物质为:A为炭、B为一氧化碳、C为二氧化碳、D为铁、E为碳酸钙、F为铜、G为为硫酸亚铁,代入检验符合题意,据此分析解答有关的问题.
解答 解:由题意可知,“A、B、C三种物质中都含有碳元素,A为黑色固体”,而A与氧气反应生成C;C可反应生成白色沉淀E;而A与氧气反应生成B;而B与氧化铁反应生成C和D,说明B具有还原性;而D与硫酸铜溶液反应生成红色固体F和G.则推测个物质为:A为炭、B为一氧化碳、C为二氧化碳、D为铁、E为碳酸钙、F为(1)由上述分析可知,F为铜,化学式为Cu,物质类别是:金属;
(2)反应①是碳充分燃烧生成了二氧化碳,反应的化学方程式是:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,反应类型为:化合反应;
(3)反应④是铁与硫酸铜反应生成了铜和硫酸亚铁,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu,该反应的实验现象是:在铁的表面有红色物质生成,溶液由蓝色逐渐变为浅绿色;
(4)为了防止装置漏气,一氧化碳通入Fe2O3前的实验操作是:检查装置的气密性;
(5)一氧化碳使人容易中毒的原因是:能与人体中的血红蛋白结合,使人体缺氧.
故答案为:(1)Cu,金属;.(2)C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,化合反应;(3)Fe+CuSO4═FeSO4+Cu,在铁的表面有红色物质生成,溶液由蓝色逐渐变为浅绿色;(4)检查装置的气密性;(5)能与人体中的血红蛋白结合,使人体缺氧.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案| A. | -3 | B. | 0 | C. | +1 | D. | +4 |
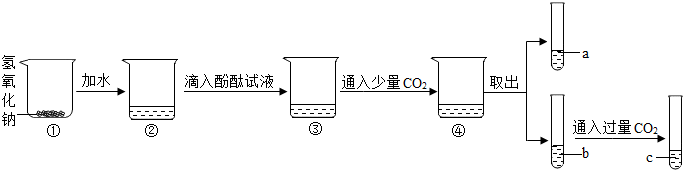
(1)用手触摸②的烧杯外壁,感觉发烫,这是由于氢氧化钠固体溶于水时会放热(填“吸热”或“放热”),该溶液呈无色;③中的溶液显红色.
(2)从③到④溶液的颜色变化不明显,说明④中的溶液呈碱性(填“酸”或“碱”).
(3)c溶液和a溶液对比,c溶液颜色更浅.
【提出问题】为什么继续通入过量的二氧化碳气体溶液颜色会更浅?
【查阅资料】(1)Na2CO3+CO2+H2O═2NaHCO3 (2)Ca(NO3)2溶液与NaHCO3溶液不反应
【设计实验】
| 实验操作 | 实验现象 | 实验结论 | |
| 甲 | 取少量c溶液滴入稀盐酸 | 产生气泡 | 溶液中含较多的CO32-或HCO3- |
| 乙 | 另取少量c溶液滴入硝酸钙溶液 | 无明显现象 | 溶液中没有大量的碳酸根离子 |
【实验反思】同种反应物在不同的条件下发生化学反应时,可能得到不同的产物.如:碳在氧气中燃烧可以生成二氧化碳或一氧化碳.
| A. | O2 | B. | KNO3 | C. | Hg | D. | H2SO4 |
| A. | 面粉加工厂“严禁烟火” | B. | 冬天用煤取暖时封闭门窗 | ||
| C. | 室内着火时,立即打开门窗通风 | D. | 到煤窑中挖煤用火把照明 |