题目内容
11. 如图是某葡萄糖酸锌口服液的标签.根据题意回答:
如图是某葡萄糖酸锌口服液的标签.根据题意回答:(1)葡萄糖酸锌中碳元素和氢元素的质量比72:11
(2)每个葡萄糖酸锌分子中共有49个原子.
(3)葡萄糖酸锌的相对分子质量是455
(4)请计算每支该口服液中葡萄糖酸锌的质量是多少?
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据每个葡萄糖酸锌分子的构成,进行分析解答.
(3)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(4)根据题意,每支该口服液中含锌6.5mg,进行分析解答.
解答 解:(1)葡萄糖酸锌中碳元素和氢元素的质量比(12×12):(1×22)=72:11.
(2)1个葡萄糖酸锌分子是由12个碳原子、22个氢原子、14个氧原子和1个锌原子构成的,则每个葡萄糖酸锌分子中共有49个原子.
(3)葡萄糖酸锌的相对分子质量为12×12+1×22+16×14+65=455.
(4)每支该口服液中含锌6.5mg,则每支该口服液中葡萄糖酸锌的质量是6.5mg÷($\frac{65}{455}$×100%)=45.5mg.
故答案为:(1)72:11;(2)49;(3)455;(4)45.5mg.
点评 本题难度不大,考查同学们结合标签新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
4.“食品安全重于泰山”,下列做法正确的是( )
| A. | 用工业盐亚硝酸钠调味--降低成本 | |
| B. | 大量使用福尔马林浸泡生鲜食品--防止腐烂变质 | |
| C. | 使用小苏打烘焙糕点--使糕点松软 | |
| D. | 霉变的花生也要食用--节约是美德 |
1.下列关于环境问题的说法正确的是( )
| A. | 防止“白色污染”,就不能使用塑料制品 | |
| B. | 用脱硫煤作燃料,可减少温室效应 | |
| C. | 汽油中加入乙醇可节省石油资源,减少污染 | |
| D. | 废旧电池只要埋入土中,就能防止其对水源的污染 |
7.下列变化过程中只发生物理变化的是( )
| A. | 铁制品接头处出现红色铁锈 | |
| B. | 以大米、高粱、小麦等粮食为原料酿酒 | |
| C. | 充入气球中氢气太多而爆炸 | |
| D. | 用氢氧焰切割金属 |
19.下列有关知识的说法,完全正确的一组是( )
| A | 化学之最 | B | 符号中数字“2”的意义 |
| 地壳中含量多的金属元素:Fe 人体中含量最多的金属元素:Ca 空气中性质最稳定的物质:N2 | 2O:两个氧分子 $\stackrel{-2}{O}$:一个氧离子带两个单位负电荷 O2:两个氧原子 | ||
| C | 化学记录 | D | 物质及其应用 |
| 托盘天平可称质量为3.62g的食盐 筒量可量取9.26mL水 pH试纸测纯碱溶液pH为12.3 | 一氧化碳可用于炼铁 食盐可作保存食品的防腐剂 碳酸氢钠可作面食发酵粉起泡剂 |
| A. | A | B. | B | C. | C | D. | D |
20.如图是钠元素和氯元素在元素周期表中的信息和有关的4种粒子结构示意图,下列说法正确的是( )
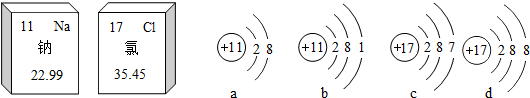
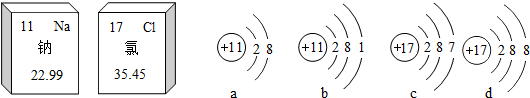
| A. | 钠、氯都属于金属元素 | B. | 氯化钠是由a,d两种粒子构成的 | ||
| C. | 氯的相对原子质量是35.45g | D. | a表示的是一种阴离子 |
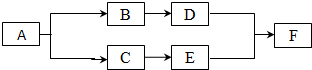 已知A-F是初中化学常见的物质,下图为这些物质的相互转化关系图.其中A在高温条件下分解为B和C两种氧化物,且B放入水中有明显的放热现象;E物质可作为工业制造玻璃的原料;F为碱,其固体敞口放置易潮解.(其中部分反应物、生成物和反应条件已省略).
已知A-F是初中化学常见的物质,下图为这些物质的相互转化关系图.其中A在高温条件下分解为B和C两种氧化物,且B放入水中有明显的放热现象;E物质可作为工业制造玻璃的原料;F为碱,其固体敞口放置易潮解.(其中部分反应物、生成物和反应条件已省略).