题目内容
19.经测定某硝酸铵样品中含氮量为31.5%,则该样品中含硝酸铵的质量分数是( )| A. | 90% | B. | 95% | C. | 35% | D. | 31.5% |
分析 混合物中某化合物的质量分数(纯度)=$\frac{含杂质物质元素的质量分数}{物质中某元素的质量分数}$×100%,进行分析解答.
解答 解:纯净的碳酸氢铵中氮元素的质量分数为$\frac{14×2}{14×2+1×4+16×3}$×100%=35%.
如果杂质不含氮元素,则硝酸铵样品的纯度为$\frac{31.5%}{35%}$×100%=90%.
故选:A.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
10.下列食物主要提供糖类的是( )
| A. | 大米 | B. | 鸡蛋 | C. | 苹果 | D. | 菠菜 |
14.有以下几种物质按一定规律排列:HCl、Cl2、KClO3、( )、KClO4请将空缺的物质选择出来是( )
| A. | MgCl2 | B. | NaCl | C. | HClO | D. | ClO3 |
4.能说明酒精溶液是混合物的( )
| A. | 溶液有特殊的气味 | B. | 溶液在空气中能燃烧 | ||
| C. | 溶液是无色的 | D. | 溶液中含有两种分子 |

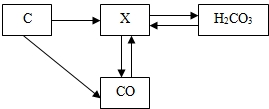 碳和部分碳的化合物间转化关系如图所示.
碳和部分碳的化合物间转化关系如图所示.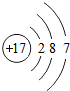 是某元素的原子结构示意图,请填写空白.
是某元素的原子结构示意图,请填写空白.