题目内容
18.许多因素会影响化学反应速率.请分析下列实验或事实,分别说明在其他条件不变时,这些因素是如何影响化学反应速率的.示例:硫在纯氧中燃烧比在空气中进行得更快,更剧烈.答:增大反应物浓度,可以加快化学反应速率.(1)同种食品在夏天比冬天更容易变质.答:升高温度,可以加快化学反应速率
(2)过氧化氢溶液在常温下能缓慢分解,若加入少量二氧化锰时分解加速.
答:使用催化剂,可以加快化学反应速率
(3)在相同质量的锌粉和锌粒中分别加入足量l0%的稀盐酸,前者先反应完.
答:增大反应物的接触面积,可以加快化学反应速率
(4)以下是某研究小组探究影响反应速率部分因素的相关实验数据.
| 实验序号 | 过氧化氢溶 液浓度/% | 过氧化氢溶液体积/mL | 温度/℃ | 二氧化锰用量/g | 收集氧气体积/mL | 反应所需 时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 |  | 2 | 49.21 |
| ④ | 30 | 5 | 55 |  | 2 | 10.76 |
②用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总重量不变(选填“减小”或“不变”或“增大”).
分析 反应物浓度越大,温度越高,接触面积越大,使用催化剂,反应速率越快;
通过对比实验,可以判断影响反应速率的因素;
只要过氧化氢溶液中溶质质量不变,完全分解后生成的氧气的质量不变.
解答 解:(1)同种食品在夏天比冬天更容易变质.答:升高温度,可以加快化学反应速率.
故填:升高温度,可以加快化学反应速率.
(2)过氧化氢溶液在常温下能缓慢分解,若加入少量二氧化锰时分解加速.答:使用催化剂,可以加快化学反应速率.
故填:使用催化剂,可以加快化学反应速率.
(3)在相同质量的锌粉和锌粒中分别加入足量l0%的稀盐酸,前者先反应完.答:增大反应物的接触面积,可以加快化学反应速率.
故填:增大反应物的接触面积,可以加快化学反应速率.
(4)①通过实验①和②对比可知,化学反应速率与反应物有关;
从实验③和④对比可知,化学反应速率与温度的关系是温度越高,反应速率越快.
故填:反应物浓度;温度越高,反应速率越快.
②用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,但是产生氧气的总重量不变.
故填:不变.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
6. 空气中主要含有氧气和氮气.某化学兴趣小组的同学用图所示装置进行空气里氧气含量的测定.实验前先用弹簧夹夹紧乳胶管,点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧.待红磷熄灭后,发现红磷还有剩余,冷却,打开弹簧夹,烧杯中的水倒流进集气瓶中,用量筒测出进入到瓶中的水的体积,记录下表中.
空气中主要含有氧气和氮气.某化学兴趣小组的同学用图所示装置进行空气里氧气含量的测定.实验前先用弹簧夹夹紧乳胶管,点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧.待红磷熄灭后,发现红磷还有剩余,冷却,打开弹簧夹,烧杯中的水倒流进集气瓶中,用量筒测出进入到瓶中的水的体积,记录下表中.
(1)实验结束后,整理数据如下(注:集气瓶容积为100mL)
分析上表中的实验记录可知第2次实验是肯定不成功的,原因之一可能是装置漏气.
(2)由表中数据可知:氧气约占空气体积的20.3%(结果保留到小数点后一位).
(3)通过本实验还可以认识集气瓶中剩余气体的性质:不支持燃烧,难溶于水(写出其中一点).
 空气中主要含有氧气和氮气.某化学兴趣小组的同学用图所示装置进行空气里氧气含量的测定.实验前先用弹簧夹夹紧乳胶管,点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧.待红磷熄灭后,发现红磷还有剩余,冷却,打开弹簧夹,烧杯中的水倒流进集气瓶中,用量筒测出进入到瓶中的水的体积,记录下表中.
空气中主要含有氧气和氮气.某化学兴趣小组的同学用图所示装置进行空气里氧气含量的测定.实验前先用弹簧夹夹紧乳胶管,点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧.待红磷熄灭后,发现红磷还有剩余,冷却,打开弹簧夹,烧杯中的水倒流进集气瓶中,用量筒测出进入到瓶中的水的体积,记录下表中.(1)实验结束后,整理数据如下(注:集气瓶容积为100mL)
| 实验次数 | 1 | 2 | 3 | 4 |
| 进入集气瓶中水的体积(mL) | 20 | 9 | 21 | 20 |
(2)由表中数据可知:氧气约占空气体积的20.3%(结果保留到小数点后一位).
(3)通过本实验还可以认识集气瓶中剩余气体的性质:不支持燃烧,难溶于水(写出其中一点).
13.如表呈现的是部分元素的原子结构示意图、主要化合价等信息.
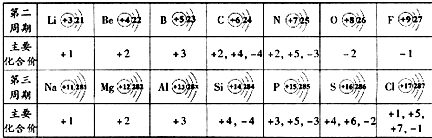
下列叙述错误的是( )

下列叙述错误的是( )
| A. | 铝原子结构示意图的最外层有3个电子 | |
| B. | 元素的正化合价数一定等于原子的最外层电子数 | |
| C. | 核电荷数分别为11和9的元素,组成化合物的化学式为NaF | |
| D. | 同一周期中,原子的核外电子层数相同,最外层电子数从左向右逐渐增多 |
10.下列化学方程式书写正确的是( )
| A. | 2Fe+6HCl═2FeCl3+3H2↑ | B. | CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+CO2 | ||
| C. | NaHCO3+HCl═NaCl+CO2↑+H2O | D. | 2NaOH+CuSO4═Na2SO4+Cu(OH)2 |
7.在植物生长的过程中,施用氮肥能使枝叶繁茂、磷肥能使果实饱满、钾肥能使茎杆健壮.种植吃叶的蔬菜(如青菜),应施用较多的化肥是( )
| A. | 微量元素肥料 | B. | NH4HCO3 | C. | K2SO4 | D. | 磷肥 |
8.下列有关数据正确的是( )
| A. | 用托盘天平称量了15.57g的食盐 | |
| B. | 给试管里液体加热,试管与桌面成45°角 | |
| C. | 酒精灯内酒精不得超过容积的$\frac{1}{3}$ | |
| D. | 取用固体药品时,未标明用量,应取1g固体 |