题目内容
2.(1)电解水时事先在水中加入少量氢氧化钠的目的是增强水的导电性.(2)在正极上得到的气体用带火星的木条 检验,证明是氧 气,在负极上得到的气体用燃着的木条 检验,证明是氢 气.同温同压下两种气体的体积比等于分子个数比,则正、负两极上得到的气体的分子个数比为1:2.
(3)根据上述事实可以得出:水是由氢元素、氧元素 组成的.此实验可以证明在化学变化中分子再分为原子,原子不能再分而是重新组合,原子是化学变化 中的最小粒子.
(4)实验中氢气和氧气的体积比略大于2/1.针对这一发现,你认为下列做法中不可取的是B
A.多次实验查找原因
B.反复 实验所得数据与理论值相差不多,可以认为实验以成功
C.大胆提出假设:氧气比氢气易溶于水
D.查找实验装置是否漏气
(5)写出电解水及氢气燃烧的文字表达式水$\stackrel{通电}{→}$氢气+氧气;氢气+氧气$\stackrel{点燃}{→}$水.
分析 (1)在做电解水的实验时,为了增强水的导电性,可在水中加入少量稀硫酸或氢氧化钠溶液;
(2)闭合电路后,会看到试管内的电极上出现气泡,过一段时间,与电源正极相连的试管产生的气体能使带火星的木条复燃,而与电池负极相连的试管产生的气体可以燃烧,它们体积比约为1:2,由此结合化学反应的实质可以判断出水的组成.
(3)水通电生成氢气和氧气,由此结合化学反应的实质可以判断出水的组成;
(4)电解水时生成氢气和氧气,由于氧气的溶解性大于氢气的溶解性,开始时氢气和氧气的体积比应略大于2:1,但随着生成的气体的增多,氢气和氧气的体积比接近2:1,如果有较大误差,就要从多方面查找原因;
(5)根据水通电生成氢气和氧气,氢气燃烧是氢气和氧气点燃生成水书写.
解答 解:(1)在做电解水的实验时,为了增强水的导电性,可在水中加入少量稀硫酸或氢氧化钠溶液;
(2)闭合电路后,会看到试管内的电极上出现气泡,过一段时间,与电源正极相连的试管产生的气体能使带火星的木条复燃,为氧气,而与电池负极相连的试管产生的气体可以燃烧,为氢气,它们体积比约为1:2,正负极上的气体所以分子数之比是1:2;
(3)水通电生成氢气和氧气,所以可以判断水是由氢元素和氧元素组成的;反应的实质水水分子再分为氢原子和氧原子,每两个氢原子重新结合成氢分子,大量的氢分子构成氢气;每两个氧原子结合构成氧分子,大量的氧分子构成氧气,所以该实验说明化学变化中分子可以再分,原子不能再分;反应前后元素的种类不变;
(4)A、试验中出现了误差,可以反复多次实验,通过分析对比查找原因,故A做法可取;
B、如果收集氧气的装置漏气,一定会使氢气和氧气的体积比大于2:1,有这种可能,故B做法可取;
C、进行化学实验,应有一种实事求是,严谨求实的科学态度,不能差不多就可以认为实验成功,故C做法不可取;
D、由于氧气的溶解性大于氢气的溶解性,氢气和氧气的体积比应略大于2:1,这种假设是成立的,故D做法可取.
(5)水通电生成氢气和氧气,反应的文字表达式为水$\stackrel{通电}{→}$氢气+氧气;氢气燃烧是氢气和氧气点燃生成水,反应的表达式为:氢气+氧气$\stackrel{点燃}{→}$水;
故答案为:(1)增强水的导电性;
(2)带火星的木条;氧;燃着的木条;氢;1:2;
(3)氢元素、氧元素;分子再分为原子,原子不能再分而是重新组合;化学变化;
(4)B;
(5)水$\stackrel{通电}{→}$氢气+氧气;氢气+氧气$\stackrel{点燃}{→}$水.
点评 解答这类题目时,首先,要熟记电解水实验的有关操作、现象、结论或推论等;以及有关的理论知识(如分子和原子的定义、区别、联系,化学反应的实质、基本类型,等等).然后,根据所给的实验、问题情景信息,或者是图示信息,结合所学的相关知识和技能,细心地探究后,按照题目要求进行选择或填写即可

 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案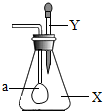 如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压胶头滴管使液体滴入瓶中,振荡,一会儿可见小气球a鼓起.X、Y可能是哪些物质?请将相应物质的化学式填入下表中:
如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压胶头滴管使液体滴入瓶中,振荡,一会儿可见小气球a鼓起.X、Y可能是哪些物质?请将相应物质的化学式填入下表中:| X | Y |
| CO2 | NaOH |
| NH3 | H2SO4 |
| A. | 制取02:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$ K2MnO4+MnO2+O2↑ | |
| B. | 制取H2:Zn+2HCl═ZnCl2+H2↑ | |
| C. | 制取C02:CaCO3+H2SO4═CaSO4+CO2↑+H2O | |
| D. | 制取02:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ |
| A. | 禁止生产、销售、使用塑料购物袋 | |
| B. | 提倡使用竹篮等传统物品代替塑料购物袋 | |
| C. | 提高废塑料的回收利用水平 | |
| D. | 研制、使用可降解的材料,如“玉米塑料”等 |

 水是生命之源,自然界的水经过不同处理后,用途更加广泛.
水是生命之源,自然界的水经过不同处理后,用途更加广泛.