题目内容
11.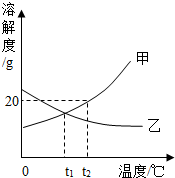 如图是甲、乙两种固体物质的溶解度曲线.下列说法中错误的是( )
如图是甲、乙两种固体物质的溶解度曲线.下列说法中错误的是( )| A. | t1℃时,甲、乙两物质的溶解度相等 | |
| B. | t2℃时,甲物质的饱和溶液中溶质的质量分数为20% | |
| C. | 甲物质的溶解度随温度升高而增大 | |
| D. | 将t2℃时乙物质的饱和溶液降温到t1℃时,溶质质量分数不变 |
分析 根据题目信息和溶解度曲线可知:甲固体物质的溶解度,是随温度升高而增大,而乙的溶解度随温度的升高而减少;t1℃时,甲、乙两物质的溶解度相等正确;t2℃时,甲的溶解度是20g,甲物质的饱和溶液中溶质的质量分数=$\frac{20g}{120g}×100%≈16.7%$,不是20%;将t2℃时乙物质的饱和溶液降温到t1℃时,溶质质量分数不变正确,因为乙溶液由饱和溶液变为不饱和溶液,质量分数不变.
解答 解:A、由溶解度曲线可知:t1℃时,甲、乙两物质的溶解度相等正确,正确但不符合题意,故选项错误;
B、t2℃时,甲的溶解度是20g,甲物质的饱和溶液中溶质的质量分数=$\frac{20g}{120g}×100%≈16.7%$,不是20%,错误符合题意,故选项正确;
C、由溶解度曲线可知:甲固体物质的溶解度,是随温度升高而增大的,正确但不符合题意,故选项错误;
D、将t2℃时乙物质的饱和溶液降温到t1℃时,溶质质量分数不变正确,因为乙溶液由饱和溶液变为不饱和溶液,质量分数不变,正确但不符合题意,故选项错误;
故选B
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
相关题目
1.某兴趣小组的同学为了探究化学反应前后反应物与生成物之间的质量关系设计了如下三个实验:
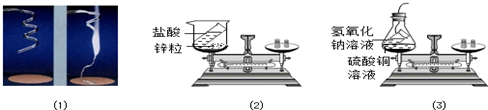
实验(1):称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量
实验(2):将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,过一会再称量.(化学方程式是:Zn+2HCl═ZnCl2+H2↑)
实验(3):将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥形瓶口塞上橡皮塞,称量,然后设法将两种溶液接触,过一会再称量.化学方程式是:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4
他们得到三次实验的数据见表:
(1)在实验①中反应后的质量比反应前明显增加了,请解释原因:根据质量守恒定律,参加反应的镁带和氧气的质量总和,等于反应后生成的氧化镁的质量,由于空气中的氧气参与了反应,因此,生成氧化镁的质量比原来镁带的质量增加了
(2)由上表中数据分析可知实验②中参加反应的氧气质量为3.2g,实验②中生成氢气的质量为0.2g.
(3)在上述三个实验中都遵循 (填“遵循”或者“不遵循”)质量守恒定律,但只有实验③(填序号) 能正确反映了反应物与生成物之间的总质量关系,因此,用实验来探究化学反应前后反应物与生成物之间的总质量关系时,当有气体参加或生成时,必须在密闭容器进行.
(4)请从分子、原子的角度解释反应前后质量相等的原因:化学反应前后原子的种类、数目和质量没有发生改变
(5)在化学反应前后,肯定不会变化的是①③④
①原子的数目 ②分子的数目 ③元素的种类 ④物质的质量总和
⑤物质的种类 ⑥物质的体积 ⑦物质的状态.

实验(1):称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量
实验(2):将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,过一会再称量.(化学方程式是:Zn+2HCl═ZnCl2+H2↑)
实验(3):将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥形瓶口塞上橡皮塞,称量,然后设法将两种溶液接触,过一会再称量.化学方程式是:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4
他们得到三次实验的数据见表:
| 编号 | 实验① | 实验② | 实验③ |
| 反应前/g | 4.8 | 112.6 | 118.4 |
| 反应后/g | 8.0 | 112.4 | 118.4 |
(2)由上表中数据分析可知实验②中参加反应的氧气质量为3.2g,实验②中生成氢气的质量为0.2g.
(3)在上述三个实验中都遵循 (填“遵循”或者“不遵循”)质量守恒定律,但只有实验③(填序号) 能正确反映了反应物与生成物之间的总质量关系,因此,用实验来探究化学反应前后反应物与生成物之间的总质量关系时,当有气体参加或生成时,必须在密闭容器进行.
(4)请从分子、原子的角度解释反应前后质量相等的原因:化学反应前后原子的种类、数目和质量没有发生改变
(5)在化学反应前后,肯定不会变化的是①③④
①原子的数目 ②分子的数目 ③元素的种类 ④物质的质量总和
⑤物质的种类 ⑥物质的体积 ⑦物质的状态.
2.在天平左、右两盘中各放一个等质量的烧杯,烧杯中分别加入等质量的足量的稀盐酸,天平平衡.向左盘烧杯中加入4g的Zn、Cu混合物,右盘烧杯中加入3.9g 氧化铜,天平再次平衡.则原Zn、Cu混合物中Zn的质量是下列中的( )
| A. | 0.75g | B. | 3.25g | C. | 3.9g | D. | 4g |
6.下列操作中,错误的是( )
| A. | 洒在桌面上的酒精燃烧起来,立即用湿抹布盖灭 | |
| B. | 在实验室里制取气体时,应先检查装置气密性,再装药品 | |
| C. | 用量筒量取一定体积的溶液时,仰视读数或俯视读数 | |
| D. | 给试管里的液体加热,试管口不能对着自己或他人 |
3.某化肥厂需大量二氧化碳生产化肥,欲购进一批石灰石(其中杂质不参加任何反应),厂家到产地取样分析以确定价格.他们取样2g,并把20g稀盐酸分四次加入.充分反应后,每次剩余固体质量见下表.
试计算:
(1)2g石灰石中含有杂质质量是0.4g;m=0.8g;n=0.4g.
(2)上述反应中共生成CO2的质量是多少?(结果保留到0.1g)
| 稀盐酸 | 剩余固体的质量 |
| 第一次加入5g | 1.4g |
| 第二次加入5g | m |
| 第三次加入5g | 0.4g |
| 第四次加入5g | n |
(1)2g石灰石中含有杂质质量是0.4g;m=0.8g;n=0.4g.
(2)上述反应中共生成CO2的质量是多少?(结果保留到0.1g)
11.建立宏观和微观之间的联系是化学学科特有的思维方式.下列对宏观事实的微观解释错误的是( )
| A. | 10mL酒精和10mL水混合后体积小于20mL,是因为分子变小了 | |
| B. | 缉毒犬能根据气味发现毒品,是因为分子在不断地运动 | |
| C. | “热胀冷缩”,是因为分子间间隔的大小随温度的改变而改变 | |
| D. | 一氧化碳和二氧化碳具有不同的化学性质,是因为构成它们的分子不同 |